Перейти к:
Особенности иммуногематологических и гематологических показателей крови донора с редким фенотипом -D-
https://doi.org/10.35754/02345730-2020-65-1-52-60
Аннотация
Введение. Настоящее исследование посвящено редкому варианту фенотипа -D-. Впервые фенотип -D- обнаружили R. Race, R. Sanger и J. G. Selwyn в 1951 г. В России фенотип -D- был впервые обнаружен Мороковым в 1985 г. Обычно фенотип -D- обнаруживают при анализе причин посттрансфузионных осложнений или гемолитической болезни новорожденных, так как у таких больных выявляется высокий титр антител к отсутствующим антигенам. В настоящем исследовании фенотип -D- был выявлен в клинической лаборатории ГУЗ «Ульяновская областная станция переливания крови» у первичного донора крови.
Цель — изучить особенности иммуногематологических и гематологических показателей крови донора с редким фенотипом -D-.
Материалы и методы. Выявление фенотипа -D- иммуногематологическими методами проводилось с помощью автоматических анализаторов. Для подтверждения фенотипа -D- использовалось молекулярное типирование ДНК. Форма эритроцитов донора с фенотипом -D- оценивалась с помощью атомно-силового микроскопа, характеристики эритроидного ростка изучались с помощью автоматического гематологического анализатора. Результаты. Фенотип -D- был выявлен у первичного донора крови. Из-за крайней редкости фенотипа -D- и вследствие отсутствия запрограммированного алгоритма валидация результатов автоматическими анализаторами проходила некорректно. Решающее значение играла визуальная оценка гелевых ID-карт персоналом. Генотипирование подтвердило отсутствие специфичностей C, c, E, e, Cw гена RHCE. Гематологические показатели донора находились в пределах возрастной нормы. Оценка изображения цитологического препарата крови донора не выявила изменений формы эритроцитов и их размера.
Заключение. Первичное определение фенотипа -D- с помощью автоматических иммуногематологических анализаторов может осложняться невозможностью валидации результатов, некорректной работой их программного обеспечения и необходимостью экспертной оценки проб крови персоналом. Рассматриваемый случай фенотипа -D- не сопряжен с изменениями формы эритроцитов и гематологических показателей крови.
Для цитирования:
Ламзин И.М., Соколова М.Н., Хайруллин Р.М., Минеева Н.В., Хапман М.Э. Особенности иммуногематологических и гематологических показателей крови донора с редким фенотипом -D-. Гематология и трансфузиология. 2020;65(1):52-60. https://doi.org/10.35754/02345730-2020-65-1-52-60
For citation:
Lamzin I.M., Sokolova M.N., Khayrullin R.M., Mineeva N.V., Khapman M.E. Features of immunohematological and hematological parameters of a donor with a rare phenotype -D-. Russian journal of hematology and transfusiology. 2020;65(1):52-60. (In Russ.) https://doi.org/10.35754/02345730-2020-65-1-52-60
Введение
В настоящее время учреждения службы крови на основании существующих нормативных документов проводят определение антигенов эритроцитов, в том числе и антигенов системы Rh, у всех доноров РФ [1]. При использовании обозначения фенотип -D- имеются в виду следующие типированные специфичности: D+, C-, c-, E-, е. Обычно фенотип -D- обнаруживают при выявлении причин посттрансфузионных осложнений или гемолитической болезни новорожденных, так как у таких больных выявляется высокий титр антител к отсутствующим антигенам [2]. В настоящем исследовании фенотип -D- был выявлен в клинической лаборатории ГУЗ «Ульяновская областная станция переливания крови» у первичного донора крови, а в последующем у его родного брата.
Впервые фенотип -D- обнаружили R. Race, R. Sanger и J.G. Selwyn в 1951 г. [3]. В России фенотип -D- был впервые обнаружен В. А. Мороковым в 1985 г. и исследован Т. М. Пискуновой и соавт. [4] при разборе клинического случая привычного невынашивания беременности женщины, также проживавшей на территории Ульяновской области. Для уточнения фенотипа было проведено молекулярное типирование ДНК исследуемого донора крови и его ближайших родственников. Кроме иммуногематологического выявления фенотипа и его генетического подтверждения были изучены некоторые показатели крови исследуемых лиц. Был проведен общий анализ крови с помощью автоматического гематологического анализатора для уточнения состояния эритроидного ростка. Для оценки формы эритроцитов в настоящей работе был применен атомно-силовой микроскоп, который ранее уже использовался для исследования качества эритроцитов донорской крови, заготовленной на базе ГУЗ «Ульяновская областная станция переливания крови» [5].
Цель — изучить особенности иммуногематологических и гематологических показателей крови донора с редким фенотипом -D-.
Материалы и методы
Исследование выполнено в ГУЗ «Ульяновская областная станция переливания крови» в соответствии с требованиями этических норм и принципов Декларации Хельсинки (1964 г.) со всеми последующими изменениями и дополнениями, а также действующего законодательства РФ. Все первичные документальные данные исследованных образцов крови были обезличены в соответствии с требованиями п. 3 ст. 6 действующего Федерального закона РФ 152-ФЗ «О персональных данных».
Для иммуногематологического исследования донора крови и его ближайших родственников (мать, отец, брат) был проведен сбор четырех образцов крови в вакуумные пробирки Vacuette с КДДТА фирмы Greiner-Bio-One (Австрия). Исследования на наличие антигенов AB0 и антигенов системы Rh (D, С, с, Е, е) проводились двумя методами. Первый метод — агглютинация эритроцитов в геле на иммуногематологическом анализаторе HEMOS SP компании Bio Rad (США). Выбор метода был обусловлен тем, что принцип гелевого метода позволяет с высокой степенью достоверности трактовать полученный результат при визуальной оценке. Второй метод — магнитизация эритроцитов на автоматизированном иммуногематологическом анализаторе QWALYS компании Diagast (Франция). Принцип метода магнитизации эритроцитов основан на использовании магнитных частиц в процессе подготовки образцов крови для исследований, которые абсорбируются на эритроцитах. Под действием магнитного поля эритроциты с абсорбированными магнитными частицами перемещаются в дно лунки и вступают в реакцию с сухим реагентом (агглютинация) [6].
Для подтверждения фенотипа было проведено молекулярное типирование ДНК [7]. Исследование проводилось в лаборатории изосерологии ФГБУ РосНИИГТ ФМБА России. Для анализа использовали лейкоцитарную ДНК, которую выделяли с помощью набора ДНК- сорб-В («Амплипрайм») из образцов крови, отобранных в вакуумные пробирки Vacuette с КДДТА фирмы Greiner-Bio-One (Австрия). Типирование проводили с помощью анализатора FluoVista. Молекулярная система детекции FluoVista основана на методе полимеразной цепной реакции (ПЦР) с аллель-специфическими праймерами SSP и флуоресцентной детекцией «по конечной точке» производства компании Inno-train Diagnostik GmbH (Германия). Детекцию флуоресценции до и после проведения ПЦР осуществляли с помощью термоциклера С1000 Touch компании Bio Rad (США).
Для оценки состояния эритроидного ростка исследуемых лиц с фенотипом -D- был проведен общий анализ крови с помощью автоматического гематологического анализатора Sysmex 1000i (Япония). Образцы капиллярной крови, полученные путем прокола скарификатором кожи дистальной фаланги пальца, отбирали в микропробирки фирмы Sarstedt-Microvttte® 200 К3 Е (Германия). Далее микропробирки устанавливали в специальные разъемы анализатора.
Исследование формы поверхности эритроцитов и их размера проводили с помощью атомно-силового микроскопа на базе лаборатории Научноисследовательского технологического института ФГБОУ ВО «Ульяновский государственный университет» Минобрнауки РФ. Атомно-силововая микроскопия — метод, основанный на измерении положения микрозонда, движущегося по поверхности образца, и обработке этой информации с помощью специальной компьютерной программы с построением изображения [8]. Для исследования образцов крови с помощью атомно-силового микроскопа готовили цитологические препараты: каплю капиллярной крови, полученную путем прокола скарификатором кожи дистальной фаланги пальца, наносили на чистое обезжиренное предметное стекло и равномерно распределяли краем пластикового шпателя. Препарат фиксировали методом высушивания на воздухе в течение 20 минут при комнатной температуре. Возможность сканирования с помощью атомно-силового микроскопа цитологических препаратов эритроцитов с фиксацией методом высушивания на открытом воздухе и получением корректных результатов приводится в работе M. Takeuchi и соавт. [9], при этом авторами отмечали, что высушивание эритроцитов практически не изменяло их форму. В данной работе использовали атомносиловой микроскоп фирмы NT-MDT (Россия), модель Solver P47-Pro. Для создания изображений образцов применяли резонансный метод с генерируемой частотой 300 kHz. Сканируемая площадь образцов составляла 120 х 120 мкм. С помощью программы NOVA строили изображения поверхности препаратов. Далее на компьютерных моделях сканированных препаратов оценивали форму эритроцитов и их размер [10].
Результаты
Первоначальная диагностика антигенной структуры эритроцитов проводилась с помощью иммуногематологических методов. На рисунке 1 представлен протокол исследования, полученный с помощью автоматизированного иммуногематологического анализатора QWALYS, на котором можно увидеть, что в образцах крови пробанда и его брата (образцы C и D) отсутствуют антигены С, с, Е, е и К. При этом анализатор при валидации проведенного фенотипирования крови донора с отсутствующими антигенами системы Rh в графе «Результат» выводит ******* (рис. 1). Аппарат корректно интерпретировал фенотипы матери и отца, содержащие антигены системы Rh (образцы А и В). Предположительно это произошло из-за того, что вследствие исключительной редкости фенотипа -D- в программное обеспечение не был заложен алгоритм интерпретации подобного результата. При проведении исследования с использованием иммуногематологического анализатора Hemos SP обнаружили похожую проблему валидации результатов. Фенотипы пробанда и его брата были расценены программой как ошибочные, и протокол зафиксировать не удалось. Для демонстрации фенотипа образца крови пробанда приводилось изображение гелевой ID-карты компании Bio Rad (рис. 2). Результаты, полученные при исследовании образцов крови с помощью иммуногематологических методов, представлены в таблице 1.

Рисунок 1. Изображение протокола исследования образцов крови пробанда и его родственников, полученного с помощью автоматического иммуногематологического анализаторе
Figure 1. The protocol of the study of blood samples from the proband and his relatives using an automatic immunohematological analyser
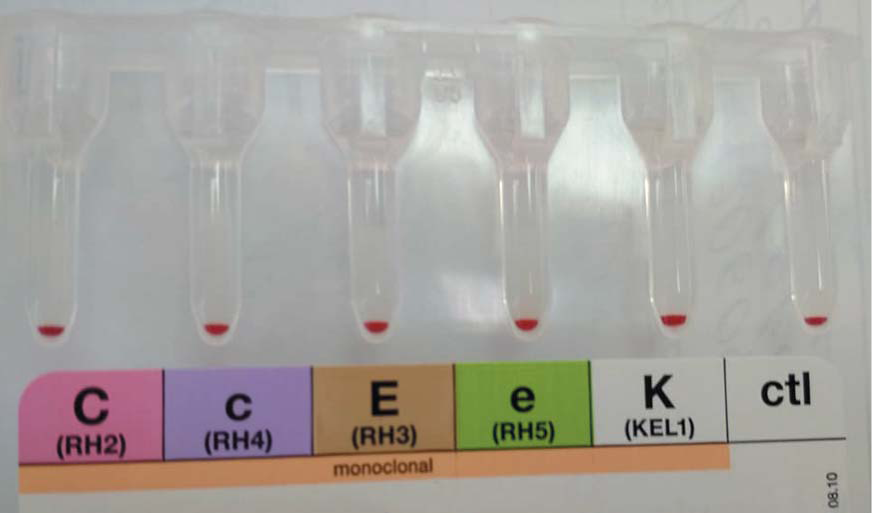
Рисунок 2. Изображение гелевой ID-карты донора с фенотипом делеций
Figure 2. The gel ID-card of the donor with the deletion phenotype
Таблица 1. Антигены эритроцитов пробанда и его родственников
Table 1. Red blood cells antigens of the proband and his relatives
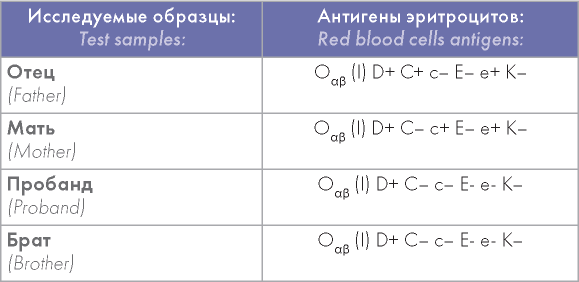
Результаты, полученные с помощью молекулярного типирования ДНК, подтвердили отсутствие специфичностей C, c, E, e, Cw гена RHCE у пробанда и его брата. Ген RHD при этом в обоих случаях присутствовал. Типирование родителей полностью подтвердило фенотипы, выявленные иммуногематологическими методами. К сожалению, техническая возможность поиска всего разнообразия вероятных аллелей гена RHCE в рамках этого исследования отсутствовала. На рисунке 3 приведена фотография протокола молекулярного типирования ДНК пробанда с помощью наборов фирмы Inno-train Diagnostik GmbH (Германия). Исходя из теории сцепленного двухгенного наследования и учитывая то, что дети, вероятно, имеют гаплотип -D- в гомозиготном состоянии, можно предположить, что родители имеют гаплотип -D- в гетерозиготном состоянии [11]. Генотип исследованных в настоящей работе лиц можно представить следующим образом: отец: CDe/-D- или Cdef-D-; мать: cde/-D- или cDe/-D-; пробанд и его брат: -D-/-D-.

Рисунок 3. Изображение протокола молекулярного типирования ДНК донора с фенотипом делеций
Figure 3. Molecular DNA typing protocol of the donor with the deletion phenotype
Для оценки состояния эритроидного ростка было проведено исследование образцов крови с помощью автоматического гематологического анализатора. Результаты стандартных гематологических показателей приведены в таблице 2. У исследуемых лиц с фенотипом -D- не выявлено отклонений показателей, характеризующих состояние эритроцитов: количество эритроцитов, концентрация гемоглобина, гематокрит, средний объем эритроцитов, среднее содержание гемоглобина в эритроците и его концентрация, стандартное отклонение и коэффициент вариации распределения популяции эритроцитов по величине находились в пределах возрастной нормы. Изображения цитологических препаратов крови пробанда и его брата, полученные с помощью атомно-силового микроскопа, подтвердили отсутствие изменений формы эритроцитов и их размера (рис. 4 и 5). Большинство эритроцитов имели двояковогнутую форму и типичный для этого типа клеток размер 7—9 мкм. Для сравнения приведено контрольное изображение цитологического препарата донора крови с фенотипом D+ С+ с— Е+ е- (рис. 6).
Таблица 2. Гематологические показатели крови пробанда и его брата
Table 2. Hematological blood indicators of the proband and his brother
|
|
RBC (1012/l) |
HGB (g/l) |
HCT (%) |
MCV (fl) |
MCH (pg) |
MCHC (g/l) |
RDW-SD (fl) |
RDW-CV (%) |
|---|---|---|---|---|---|---|---|---|
|
Пробанд (Proband) |
5,45 |
155 |
44,4 |
81,5 |
28,4 |
349 |
39,0 |
13,4 |
|
Брат (Brother) |
5,29 |
154 |
42,7 |
80,7 |
29,1 |
361 |
40,8 |
14,0 |

Рисунок 4. Изображение цитологического препарата крови пробанда, полученное с помощью атомно-силового микроскопа
Figure 4. An atomic force microscope image of a cytological blood preparation from the proband
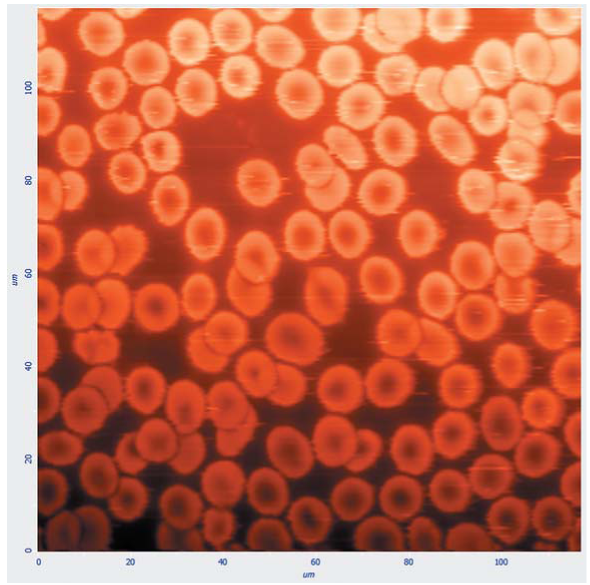
Рисунок 5. Изображение цитологического препарата крови брата пробанда, полученное с помощью атомно-силового микроскопа
Figure 5. An atomic force microscope image of a cytological blood preparation from the proband's brother
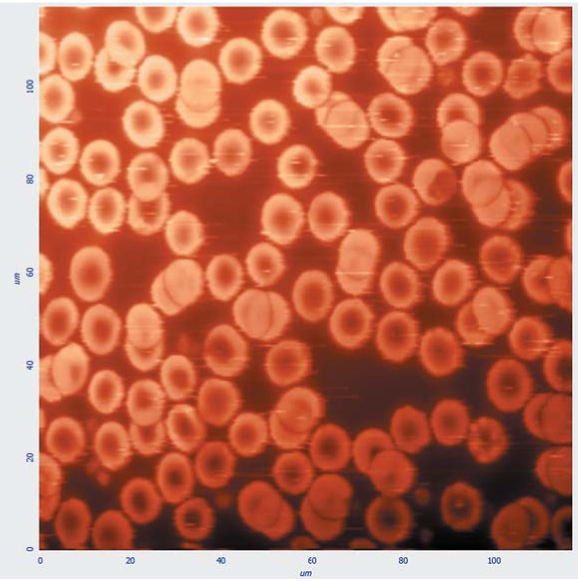
Рисунок 6. Изображение цитологического препарата крови донора с фенотипом D+ С+ с- Е+ е-, полученное с помощью атомно-силового микроскопа
Figure 6. An atomic force microscope image of a cytological blood preparation from a donor with the phenotype D+ С+ с- Е+ е-
Обсуждение
В настоящей работе продемонстрированы особенности выявления фенотипа -D- с помощью современного оборудования и интерпретации полученных результатов специализированным программным обеспечением. Несмотря на укомплектованность современных центров крови и лечебных учреждений соответствующими анализаторами, квалификация и опыт персонала могут сыграть решающую роль в принятии решений в нетипичных ситуациях. В случаях ошибок, выявляемых в работе автоматической аппаратуры иммуногематологических лабораторий, необходимо производить визуальную оценку гелевых ID-карт и анализ полученных результатов.
Учитывая редкость выявления фенотипа -D-, представлялось интересным проанализировать этиологию его возникновения. По данным R. Race и R. Sanger [12ф у большинства выявленных лиц с фенотипом -D- родители состояли в родстве. При подробном сборе анамнеза у родителей пробанда выявлено, что их близкие родственники проживают на территории небольшого населенного пункта Ульяновской области, в котором они познакомились и создали семью. Принимая во внимание тот факт, что традиционно представители национальности, к которой принадлежат оба родителя, вступают в брак предпочтительно с представителями той же национальности, предположение о дальнем родстве родителей исследуемых лиц полностью исключить невозможно. Это может объяснять наличие у обоих родителей редкого гаплотипа -D-.
Антигены системы Rh являются структурными частями мембраны эритроцитов и принимают участие в обменных процессах, а их полное отсутствие, так называемый фенотип Rhni , сопровождается изменением формы эритроцитов и склонностью к гемолизу [13]. Проведенные исследования образцов крови с помощью автоматического гематологического анализатора и атомно-силового микроскопа не выявили изменений эритроидного ростка и формы эритроцитов. Отсутствие патологии мембраны эритроцитов в рассматриваемом случае, вероятно, связано с наличием других специфичностей системы Rh.
Наличие редкого фенотипа -D- сопровождается опасностью выработки высокого титра антиэритроцитарных аллоантител к отсутствующим антигенам C, с, E, e, Cw при трансфузии донорских эритроцитов [14].
В связи с этим для исключения потенциальной иммунизации исследуемым лицам было рекомендовано проведение процедуры аутодонорства с последующим замораживанием эритроцитов. Этот метод позволяет хранить эритроциты в течение нескольких лет и осуществлять аутотрансфузию в случае возникновения показаний.
Таким образом, первичное определение фенотипа -D- с помощью автоматических иммуногематологических анализаторов может осложняться невозможностью валидации результатов, некорректной работой их программного обеспечения и необходимостью экспертной оценки проб крови персоналом. Рассматриваемый случай фенотипа -D- не сопряжен с изменениями формы эритроцитов и гематологических показателей крови.
Список литературы
1. Постановление Правительство Российской Федерации от 22 июня 2019 г. № 797 «Об утверждении правил заготовки, хранения, транспортировки и клинического использования донорской крови и ее компонентов».
2. Донсков С.И., Мороков В.А. Группы крови человека: Руководство по иммуносерологии. М.: ИП Скороходов В.А., 2011. 243 с.
3. Race R., Sanger R., Selwyn J.G. A possible deletion in a human Rh chromosome: a serological and genetical study. Brit. J. Exp. Path. 1951; 32: 124–35.
4. Пискунова Т.М., Мороков В.А., Шамшина Н.М., Тананов А.Т., Зотиков Е.А. Редкий генотип системы Резус Rh (-D-/-D). Гематология и трансфузиология. 1988; 34(10): 45–47.
5. Lamzin I, Khayrullin R. The quality assessment of stored red blood cells probed using atomic force microscopy. Anat Res Int. 2014; 869683. DOI:10.1155/2014/869683.
6. Минеева Н.В., Бутина Е.В. Иммуногематологическое обследование доноров крови и (или) ее компонентов и реципиентов: Методологические указания. СПб., 2017. 45 с.
7. Каландаров Р.С., Головкина Л.Л., Васильева М.Н. и др. Генотипирование групп крови систем АВО и резус у пациентов после множественных гемотрансфузий. Онкогематология. 2017; 12(2): 70–9. DOI: 10.17650/18188346-2017-12-2-70-79.
8. Горшкова Е., Плескова С., Михеева Э. Атомно-силовая микроскопия клеток крови человека. Наноиндустрия. 2012; 34(4): 50–3.
9. Takeuchi M, Miyamoto H, Sako Y. et al. Structure of the erythrocyte membrane skeleton as observed by atomic force microscopy. Biophys J. 1998; 74(5): 2171–83.
10. Ламзин И.М., Хайруллин Р.М., Хапман М.Э. Оценка структуры популяции эритроцитсодержащих сред, находящихся на хранении в банке крови, по данным атомно-силовой микроскопии. Вестник современной клинической медицины. 2014; (7): 16–20.
11. Tippett P. Rh Blood group system: genes 1,2 or 3? Biotest Bulletin. 1997; 5: 393–8.
12. Race R., Sanger R. Blood Groups in Man. 6-th ed. Blackwell scientific publications. 1975. 659 p.
13. Cartron, J.P. RH blood group system and molecular basis of Rh-deficiency. Best Pract Res Clin Haematol. 1999; 12(4): 655–89. DOI: 10.1053/beha.1999.0047.
14. Оловникова Н.И., Николаева Т.Л., Митерев Г.Ю. Иммуногематологическое обследование больных перед трансфузией донорских эритроцитов: пути оптимизации и улучшения качества тестирования. Справочник заведующего КДЛ. 2014; (6): 34–6.
Об авторах
И. М. ЛамзинРоссия
Ламзин Иван Михайлович – кандидат медицинских наук, заведующий отделением заготовки крови и ее компонентов.
432017, Ульяновск
М. Н. Соколова
Россия
Соколова Марина Николаевна – врач клинической лабораторной диагностики высшей категории, заведующая клинической лабораторией.
432017, Ульяновск
Р. М. Хайруллин
Россия
Хайруллин Радик Магзинурович – доктор медицинских наук, профессор, заведующий кафедрой анатомии человека.
432017, Ульяновск
Н. В. Минеева
Россия
Минеева Наталья Витальевна – доктор биологических наук, профессор, руководитель лаборатории изосерологии.
191024, Санкт-Петербург
М. Э. Хапман
Россия
Хапман Марат Эрикович – кандидат медицинских наук, главный врач.
432017, Ульяновск
Рецензия
Для цитирования:
Ламзин И.М., Соколова М.Н., Хайруллин Р.М., Минеева Н.В., Хапман М.Э. Особенности иммуногематологических и гематологических показателей крови донора с редким фенотипом -D-. Гематология и трансфузиология. 2020;65(1):52-60. https://doi.org/10.35754/02345730-2020-65-1-52-60
For citation:
Lamzin I.M., Sokolova M.N., Khayrullin R.M., Mineeva N.V., Khapman M.E. Features of immunohematological and hematological parameters of a donor with a rare phenotype -D-. Russian journal of hematology and transfusiology. 2020;65(1):52-60. (In Russ.) https://doi.org/10.35754/02345730-2020-65-1-52-60











































