Перейти к:
Преимущества и недостатки порт-систем, установленных бедренным доступом, у гематологических больных с синдромом верхней полой вены
https://doi.org/10.35754/0234-5730-2020-65-4-403-416
Аннотация
Введение. У больных с синдромом верхней полой вены альтернативным сосудистым доступом является катетеризация бедренной вены. Имеются лишь единичные сообщения об установке порт-систем бедренным доступом.
Цель — определить преимущества и недостатки порт-систем, установленных бедренным доступом, у гематологических больных с синдромом верхней полой вены.
Материалы и методы. В проспективное нерандомизированное одноцентровое исследование включено 163 больных гематологическими заболеваниями, которым установили 72 порт-системы в верхнюю полую вену, 35 порт-систем в нижнюю полую вену и 156 нетуннелируемых катетеров в бедренную вену. Регистрировали особенности катетеризации, осложнения, длительность использования, причины удаления порт-систем и катетеров.
Результаты. Не выявлено значимых различий при использовании порт-систем в верхней и нижней полых венах в частоте применения урокиназы при дисфункции катетера, дислокации катетера, возникновения катетер-ассоциированной инфекции кровотока, инфекции подкожного кармана. Различия выявлены в вероятности возникновения катетер-ассоциированного тромбоза, который при использовании бедренного доступа определялся чаще (17,0 %, или 0,9/1000 катетеро-дней, против 8,3 %, 0,2/1000 катетеро-дней, р = 0,017). Порт-системы в нижней полой вене использовали в течение меньшего времени, чем в верней полой вене (р = 0,0001). При сравнении установленных бедренным доступом нетуннелируемых катетеров и порт-систем при использовании нетуннелируемых катетеров выявлялись катетер-ассоциированные тромбозы (9/1000 против 0,9/1000 катетеро-дней, р = 0,002) и катетерассоциированная инфекция (4,9/1000 против 0,3/1000 катетеро-дней, р = 0,002). На все время лечения лимфомы требовалась одна порт-система либо от 1 до 14 (медиана — 3) нетуннелируемых катетеров, установленных бедренным доступом.
Заключение. Установка порт-системы через бедренную вену — это вынужденная мера у больных с синдромом верхней полой вены. Она имеет преимущества по частоте катетеризаций, инцидентности инфекционных и тромботических осложнений по сравнению с нетуннелируемыми катетерами, установленными бедренным доступом.
Ключевые слова
Для цитирования:
Галстян Г.М., Спирин М.В., Дроков М.Ю., Костина И.Э., Мангасарова Я.К. Преимущества и недостатки порт-систем, установленных бедренным доступом, у гематологических больных с синдромом верхней полой вены. Гематология и трансфузиология. 2020;65(4):403-416. https://doi.org/10.35754/0234-5730-2020-65-4-403-416
For citation:
Galstyan G.M., Spirin M.V., Drokov M.Yu., Kostina I.E., Mangasarova Ya.K. Advantages and disadvantages of femoral port systems in hematоlogical patients with superior vena cava syndrome. Russian journal of hematology and transfusiology. 2020;65(4):403-416. (In Russ.) https://doi.org/10.35754/0234-5730-2020-65-4-403-416
Введение
Полностью имплантируемая порт-система — это устройство сосудистого доступа, устанавливаемое больным, которым требуется долгосрочное внутривенное введение лекарственных препаратов, не предназначенных для инфузии в периферические вены, либо больным, у которых отсутствует периферический венозный доступ. Первый прототип порт-системы был разработан в 1979 г. онкологом D. Ensminger и представлял собой титановое устройство с силиконовой перегородкой и катетером из силастика. Порт-системы, прежде всего, предназначались для лечения больных раком молочной железы. Однако Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (Food and Drug Administration, FDA) потребовало от разработчиков больше убедительных доказательств об эффективности этих систем. D. Ensminger отправил в FDA образец порт-системы вместе с данными о больных, которые уже пользовались этими устройствами [1]. В 1982 г. FDA одобрило использование порт-систем, и была опубликована первая работа по применению порт-систем у онкологических больных [2]. За прошедшие десятилетия основные принципы устройства порт-систем мало изменились. В настоящее время только в США ежегодно устанавливается более 15 миллионов порт-систем [3].
Имплантация порт-систем показана больным, нуждающимся в длительном прерывистом венозном доступе. Это больные, получающие химиотерапию, трансфузии компонентов крови, факторы свертывания крови и другие виды лечения. Сравнение порт-систем с туннелируемыми катетерами Хикмана при проведении в амбулаторном режиме химиотерапии у онкологических больных показало, что порт-системы безопаснее: при их использовании реже возникали инфекционные осложнения (0,86/1000 против 2,54/1000 катетеро-дней), поломки и дислокации катетера, они в 5 раз реже удалялись из-за осложнений, чем катетеры Хикмана. В исследовании O. Wu и соавт. [4] у онкологических больных из-за осложнений преждевременно были удалены 28 % катетеров Хикмана и лишь 4 % порт-систем. Качество жизни (вождение машины, гигиена, риск инфекции, физические упражнения, риск повредить устройство) было выше у больных с порт-системами, чем с катетерами Хикмана. При проведении химиотерапии у онкологических больных через три вида катетеров (порт-системы, периферически имплантируемые катетеры и нетуннелируемые катетеры) наименьшая частота осложнений была при использовании порт-систем (2,2, 40 и 27,5 % соответственно) [5]. В двух исследованиях у больных, получавших химиотерапию, общие затраты на катетеры Хикмана оказались больше, чем на порт-системы [4, 6]. При сравнении с периферически имплантируемыми катетерами в случаях их краткосрочного использования стоимость порт-систем была больше, однако при использовании их в течение более 12 месяцев затраты на порт-системы сравнялись с затратами на периферически имплантируемые центральные катетеры [5].
Как правило, порт-системы устанавливают через одну из вен бассейна верхней полой вены: внутреннюю яремную вену, подключичную вену, наружную яремную вену, плечевую вену, подкрыльцовую вену, латеральную подкожную или медиальную подкожную вену. Однако у некоторых больных по различным причинам порт-систему невозможно установить в верхнюю полую вену. К таким причинам относятся синдром верхней полой вены у больных лимфомами [7][8], состояние после билатеральной мастэктомии [8][9][10][11][12], синдром верхней полой вены вследствие ее окклюзии метастазами в средостение при раке различной локализации [12][13][14], сдавление верхней полой вены опухолью при первичной медиастинальной лимфоме [15], планируемая лучевая терапия на область грудной клетки [10][13], измененные кожные покровы или билатеральный постлучевой дерматит на грудной клетке [8], смещение органов средостения и сосудисто-нервного пучка после пульмонэктомии у больных туберкулезом [12], гипоплазия вен бассейна верхней полой вены [18], косметические соображения. В этих случаях возникает необходимость в установке порт-системы через бедренную вену в нижнюю полую вену. Опыт установки и использования порт-систем с подобной локализацией в мире небольшой, как правило, сообщения носят либо казуистический характер, либо наблюдения ограничиваются несколькими десятками больных [8][10][15][17][18][19].
Цель настоящей работы — определить преимущества и недостатки порт-систем, установленных бедренным доступом в нижнюю полую вену, для обеспечения сосудистого доступа у онкогематологических больных с синдромом верхней полой вены.
Больные и методы
Дизайн работы — проспективное нерандомизированное одноцентровое исследование. Проведен анализ особенностей имплантации порт-систем бедренным доступом в нижнюю полую вену, причин их установки, осложнений. Для оценки влияния локализации порт-системы на возникновение осложнений сравнили результаты использования порт-систем, установленных в нижнюю или верхнюю полую вену. Для оценки влияния вида сосудистого устройства на возникновение осложнений при одном и том же доступе сравнили результаты использования порт-систем, установленных бедренным доступом, и нетуннелируемых катетеров, установленных бедренным доступом.
Больные. В исследование были включены 163 больных гематологическими заболеваниями (107 женщин и 56 мужчин) возрасте от 18 до 73 лет (медиана — 36 лет), которым установили два вида центральных венозных катетеров: 103 больным были установлены порт-системы, 60 больным установили 156 нетуннелируемых центральных венозных катетеров в бедренную вену. Всего 107 порт-систем установили 103 больным либо в верхнюю полую вену (72 порт-системы), либо в нижнюю полую вену (35 порт-систем), четверым больным порт-системы устанавливали дважды. Большую часть включенных в исследование составили больные лимфомами, реже — острыми лейкозами, в единичных случаях — другими гематологическими заболеваниями (табл. 1).
Таблица 1. Распределение больных в зависимости от нозологии
Table 1. Nosological patient profile
Диагноз Diagnosis | Число больных, n (%) Number of patients, n (%) |
Лимфома Ходжкина Hodgkin lymphoma | 12 (7,4) |
Неходжкинская лимфома Non-Hodgkin lymphoma | 105 (64,4) |
Острые лейкозы Acute leukemias | 37 (22,7) |
Острый миелоидный лейкоз Acute myeloid leukemia | 13 (8,0) |
Острый лимфобластный лейкоз Acute lymphoblastic B-leukemia | 24 (14,7) |
Множественная миелома Multiple myeloma | 2 (1,2) |
Другие онкогематологические заболевания Other haematological malignancies | 3 (1,8) |
Наследственные коагулопатии Congenital coagulopathy | 4 (2,5) |
Всего Total | 163 (100) |
Катетеры. Показаниями к установке порт-систем было проведение химиотерапии или заместительной терапии факторами свертывания в амбулаторных условиях, для которой был необходим центральный венозный доступ и/или отсутствовал периферический венозный доступ. Лишь у двух больных показаниями к установке порт-систем явилось введение факторов свертывания крови и/или компонентов крови. Если не было противопоказаний, больным устанавливали порт-систему в верхнюю полую вену яремным или подключичным доступом.
При наличии у больных синдрома верхней полой вены, стеноза или тромбоза обеих подключичных и яремных вен или брахиоцефальных стволов, не позволявших катетеризировать верхнюю полую вену, использовали бедренный сосудистый доступ. Больным имплантировали порт-системы бедренным доступом в нижнюю полую вену (порт-системы PowerPort®, Bard Access System, США и Celsite®, B. Braun Medical Inc., Германия), либо устанавливали в бедренную вену нетуннелируемые двухпросветные катетеры 7 Fr (Certofix Duo, B. Braun Medical Inc.). Нетуннелируемые катетеры не предназначены для амбулаторного лечения, поэтому после проведения очередного курса химиотерапии перед выпиской из стационара катетеры удаляли и устанавливали заново при последующей госпитализации.
Выбор размера катетера порт-системы определялся планируемым объемом терапии и диаметром пунктируемой вены: диаметр катетера не должен был превышать 45 % диаметра вены [16]. Диаметр установленных бедренным доступом катетеров порт-систем был в 11 случаях 6 Fr, в 1 случае — 7 Fr, в 23 случаях — 8 Fr. Катетеры порт-систем, установленные в верхнюю полую вену, были диаметром 6 Fr в 8 случаях и 8 Fr — в 64 случаях. У большинства больных использовали порт-системы с открытым дистальным концом катетера. У 6 больных были установлены бедренным доступом порт-системы, снабженные на дистальном конце катетера клапаном Грошонга (Bard PowerPort, Bard Access System), а у 1 больной — порт-система с лепестковым клапаном на дистальном конце катетера (Celsite® Concept Access Port System, B. Braun Medical Inc.), предполагая, что это предотвратит попадание крови в резервуар при принятии больными вертикального положения.
Установка порт-систем. Порт-системы устанавливали в процедурной, оснащенной С-дугой. После обработки операционного поля с помощью высокочастотного линейного ультразвукового датчика с частотой 10 МГц (ультразвуковой аппарат Toshiba Viamo SSA-640A, Toshiba Medical Systems Corporation, Япония) выводили изображение вены по короткой оси, пунктировали вену иглой. Успешную пункцию вены подтверждали беспрепятственным поступлением венозной крови в шприц. Вену катетеризировали по модифицированной технике Сельдингера с разламывающимся интродьюсером [1][17]. В иглу вводили J-образный металлический проводник, иглу извлекали. У входа проводника в кожу выполняли скальпелем горизонтальный разрез (1,5–3 см), который расширяли в подкожной клетчатке с помощью зажима. В месте предполагаемого расположения камеры порт-системы в подкожной клетчатке над фасцией тупым способом делали карман, соответствовавший размеру камеры. Карман делали в области, имевшей под собой плотную костную основу: при установке порт-систем в верхнюю полую вену камеру формировали в подключичной области на передней поверхности грудной клетки, при установке порт-систем бедренным доступом карман формировали на 15–20 см ниже пупартовой связки на передней поверхности бедра. Толщина тканей над поверхностью камеры составляла 0,5–1,5 см. Катетер надевали на штуцер камеры порт-системы и закрепляли с помощью предусмотренного фиксирующего устройства. Камеру погружали в карман. Надевали дистальный конец катетера на конец туннелера и проводили его сквозь подкожно-жировую клетчатку, протягивая катетер к месту входа в вену J-проводника. С помощью иглы Губера заполняли порт-систему раствором 0,9%-го натрия хлорида. По проводнику вращательными движениями вводили расширитель сосуда и интродьюсер как единое целое. Удаляли расширитель сосуда. Вводили катетер в просвет интродьюсера и проводили на необходимую глубину. При установке порт-системы через вены бассейна верней полой вены дистальный конец катетера позиционировали у каваатриального соединения, при установке бедренным доступом — в нижней полой вене, ниже отхождения почечных вен (рис. 1). Разрезы послойно ушивали. Швы снимали на 3–4-й неделе.
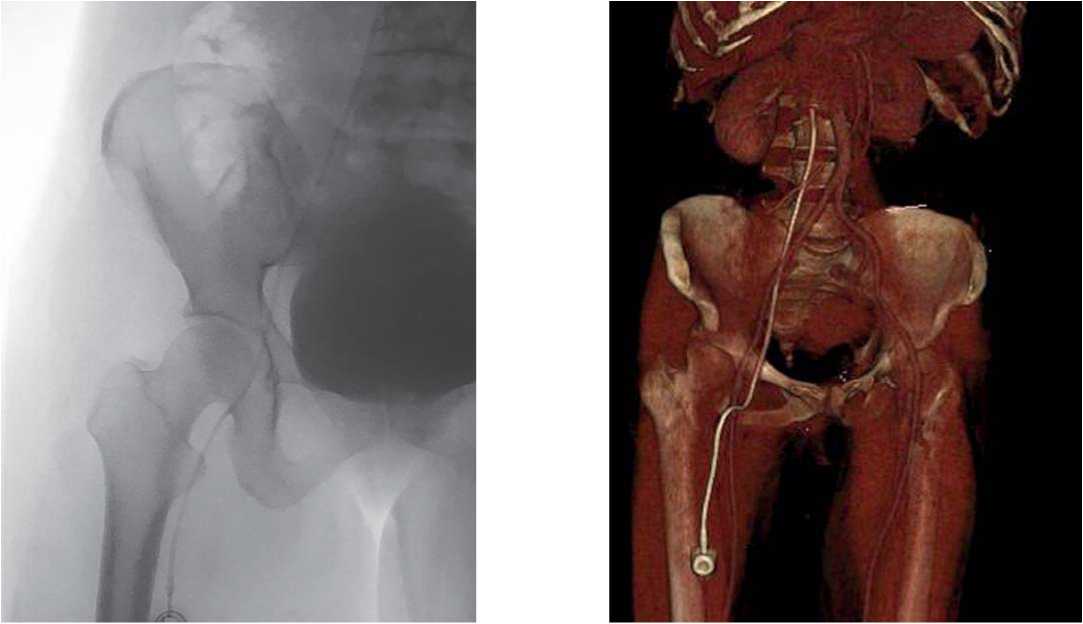
Рисунок 1. Порт-система в нижней полой вене, камера на бедре (собственное наблюдение)
Figure 1. Femoral port in vena cava inferior (own observation)
Нетуннелируемые двухпросветные катетеры Certofix Duo 7 устанавливали в процедурной. Под контролем ультразвука пунктировали бедренную вену иглой ниже пупартовой связки. Успешную пункцию вены подтверждали беспрепятственным поступлением венозной крови в шприц. Вену катетеризировали по технике Сельдингера.
Все порт-системы и нетуннелируемые катетеры были прослежены от момента установки до их удаления. Регистрировали:
- особенности проведения и позиционирования катетера порт-системы;
- ранние осложнения, обусловленные процедурой катетеризации: гематомы, случайная пункция артерии, пневмоторакс;
- поздние осложнения, возникшие в процессе эксплуатации катетера: катетер-ассоциированную инфекцию кровотока, катетер-ассоциированные тромбозы, инфекцию кармана, дислокацию камеры;
- функционирование различных порт-систем (нарушения функции, обструкция, невозможность инъекции и/или аспирации крови);
- длительность использования порт-систем;
- причины удаления порт-систем.
Под катетер-ассоциированным тромбозом понимали сочетание клинических (гиперемия, отек, боль, усиление подкожного сосудистого рисунка) и инструментальных (выявление при ультразвуковом исследовании в просвете сосуда гиперэхогенного образования, препятствующее смыканию стенок вен при компрессии датчиком, дефект контрастирования сосудов при исследовании доплеровском режиме, при ангиографии) признаков тромбоза в месте установки катетера или на протяжении сосуда.
Под катетер-ассоциированной инфекцией кровотока понимали выявление положительной культуры в образце крови, взятом из катетера на 2 и более часа раньше, чем в образце крови, взятом из периферической вены, или рост микроорганизмов при микробиологическом исследовании дистального конца катетера в сочетании с клиническими признаками (лихорадка с/без озноба) и анамнестических данных (длительность эксплуатации катетера, связь с инфузией).
Статистический анализ данных проводили с использованием статистического пакета IBM SPSS v. 23 (США). Для проверки нормальности распределения был использован критерий Шапиро — Уилка. Для оценки вероятности катетер-ассоциированной инфекции кровотока, катетер-ассоциированного тромбоза, дисфункции катетера был использован метод Каплана — Мейера. Для сравнения двух кривых применялся логранговый критерий. Для оценки влияния различных независимых факторов была использована модель пропорциональных рисков Кокса. Для оценки ранних и поздних осложнений был использован показатель инцидентности событий на 1000 катетеро-дней [23]. Данные представлены в виде медианы, минимального и максимального значений, частоты возникновения, показателя инцидентности. Порог статистической значимости р был принят равным 0,05.
Результаты
Установка порт-систем бедренным доступом. В условиях ультразвукового контроля во всех случаях бедренная вена была пунктирована с первой попытки, случайных пункций артерии не было. Предпочтение при пункции отдавали правой бедренной вене (29 больных), поскольку при проведении катетера из правой бедренной вены в нижнюю полую вену меньше изгиб и короче путь, чем из левой бедренной вены. В 6 случаях катетеризировали левую бедренную вену. В 3 случаях возникли сложности при проведении силиконового катетера по интродьюсеру вследствие его изгиба и сдавления связками, в одном случае возникла необходимость смены интродьюсера на другой, большего размера.
При установке катетера порт-системы в нижнюю полую вену использовали рентгеноскопию, поскольку в 35,3 % случаев возникли сложности при продвижении мягкого катетера: катетеры «уходили» в контралатеральную наружную подвздошную вену (11,7 %), в одну из печеночных вен (5,8 % случаев), почечную вену (5,8 %), в одну из мелких вен малого таза (12 %) (рис. 2).
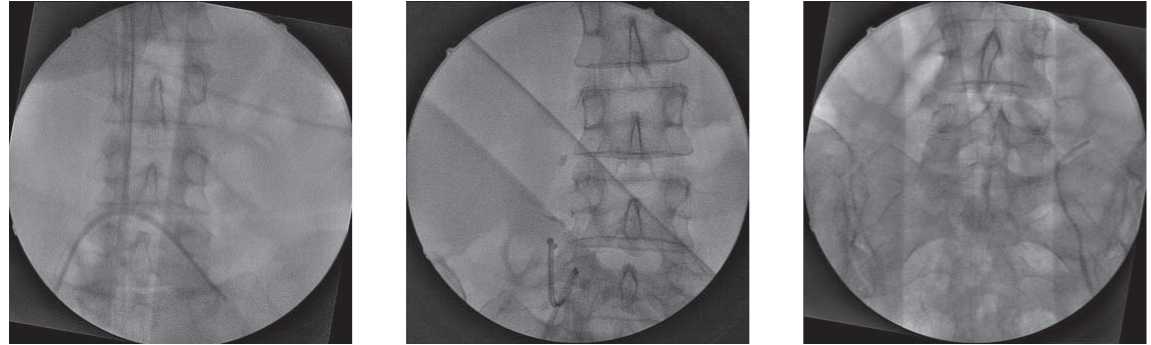
Рисунок 2. Неправильные позиции катетера при проведении в нижнюю полую вену (собственные наблюдения)
Figure 2. Incorrect catheter positioning during placement in vena cava inferior (own observation)
 Рисунок 3. Контраст, введенный через порт-систему в катетер, поступает не в нижнюю полую вену, а в один из ее притоков
Рисунок 3. Контраст, введенный через порт-систему в катетер, поступает не в нижнюю полую вену, а в один из ее притоков
Figure 3. Port-injected contrast passes through catheter into small venous branch instead of vena cava inferior
Убеждались, что дистальный конец катетера порт-системы расположен в нижней полой вене, ниже устья почечных вен, чуть выше слияния подвздошных вен [12]. Для этого вводили контраст в катетер и по его току убеждались в правильном положении катетера. Без введения контраста у одного больного после установки порт-системы в нижнюю полую вену на второй день обратили внимание на плохой ток крови при аспирации через иглу из резервуара порт системы. При введении водорастворимого контраста в катетер было обнаружено, что дистальный конец катетера находится в одном из мелких притоков нижней полой вены, собирающей кровь от поясничных вен, катетер был установлен заново.
Катетер-ассоциированная инфекция кровотока была у 2 (5,7 %) из 35 больных, инфекция подкожного кармана — у 3 (8,6 %) больных. Инфекционные осложнения были вызваны преимущественно грамположительными микроорганизмами (Staphylococcus epidermidis — 2, Staphylococcus aureus — 2, Streptococcus oralis — 1, Streptococcus parasanguinis — 1), в 1 случае — грамотрицательной палочкой (Klebsiella pneumoniаe). При выявлении положительной гемокультуры без признаков инфицирования подкожного кармана порт-системы были санированы с использованием антимикробных замков.
Катетер-ассоциированные тромбозы были выявлены при регулярном ультразвуковом исследовании у 6 (17 %) из 35 больных. Лишь в 1 случае имелись клинические проявления тромбоза глубоких вен, у 5 больных обнаружены «немые» бессимптомные пристеночные тромбы в бедренной вене, распространявшиеся вдоль катетера. Они не потребовали удаления порт-систем и полностью разрешились на проводимой антикоагулянтной терапии.
Дисфункция катетера, потребовавшая применения тауролока с урокиназой, возникла у 6 из 35 больных. Наличие клапанов на дистальном конце катетера не предотвращало возникновения дисфункции.
К моменту проведения анализа продолжали использовать 8 из 35 порт-систем, 22 порт-системы были удалены в связи с завершением лечения. У 3 больных порт-системы были удалены из-за инфекции подкожного кармана, из них у двух больных инфекция кармана сочеталась с катетер-ассоциированным тромбозом бедренной вены и катетер-ассоциированной инфекцией, причем у одного из них причиной явилась его некомплаентность (синдром Дауна), нарушение гигиенических норм. В 1 случае порт-система была удалена в связи с клинически выраженным катетер-ассоциированным тромбозом бедренной вены без признаков инфекции, еще в 1 случае порт-система была удалена в связи с дисфункцией, когда после введения контраста выяснилось, что ее катетер находится в одной из мелких вен. Длительность использования порт-систем колебалась от 37 до 465 дней (медиана — 160 дней).
В результате противоопухолевого лечения полное разрешение синдрома верхней полой вены зарегистрировано у 27 (77,1 %) больных, частичное — у 3 (8,6 %) больных, сдавление и тромбозы в крупных венозных сосудах бассейна верней полой вены сохранились у 5 (14,3 %) больных.
Больные отмечали удобство использования порт-систем. Камера порт-системы, расположенная на бедре, была удалена от паховой области, что позволяло осуществлять гигиенические процедуры. Больные сами могли легко вставить иглу в камеру порт-системы, промывать ее при необходимости. Порт системы не ограничивали физической активности больных (рис. 4).
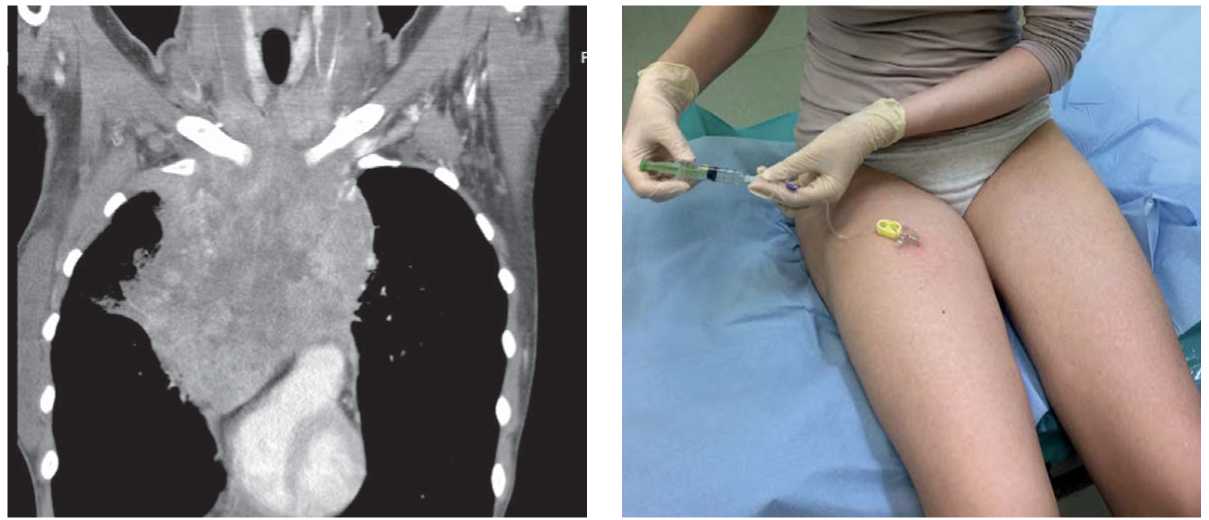
Рисунок 4. Больная первичной медиастинальной В-крупноклеточной лимфомой и с синдромом верхней полой вены, самостоятельно промывающая порт-систему на бедре
Figure 4. A patient with primary mediastinal large B-cell lymphoma and superior vena cava syndrome flushing the femoral port
Сравнение порт-систем, установленных в верхнюю и нижнюю полую вену. Сопоставлены механические и поздние осложнения при использовании 72 порт-систем, установленных в верхнюю полую вену яремным или подключичным доступом, и 35 порт-систем, установленных в нижнюю полую вену бедренным доступом (табл. 2).
Таблица 2. Сравнительная характеристика поздних и механических осложнений при эксплуатации порт-систем
Table 2. Comparison of late and mechanical complications in patients with ports
Осложнения Complications | Сосудистый доступ Vascular access | ||
порт-системы, установленные яремным или подключичным доступом (n = ٧٢) ports implanted by jugular or subclavian access (n = 72) | порт-системы, установленные бедренным доступом (n = ٣٥) femoral ports (n = ٣٥) | ||
Механические Mechanical | Дисфункция катетера (применение урокиназы), n Catheter dysfunctions (use of urokinase), n (%, per 1000 catheter days) | 12 (16,7 %, 0,4) | 6 (17 %, 0,9) |
Дислокация катетера, n (%, случаи на 1000 катетеро-дней) Catheter dislocation, n (%, per 1000 catheter days) | 2 (2,8 %, 0,06) | 1 (2,6 %, 0,15) | |
Поздние Late | Катетер-ассоциированная инфекция кровотока, n CRBSI, n (%, per 1000 catheter days) | 4 (5,6 %, 0,13) | 2 (5,7 %, 0,3) |
Инфекция подкожного кармана, n Port pocket infection, n (%, per 1000 catheter days) | 3 (4,2 %, 0,1) | 3 (8,6 %, 0,4) | |
Катетер-ассоциированный тромбоз, n Catheter-related thrombosis, n (%, per 1000 catheter days) | 6 (8,3 %, 0,2) | 6 (17,0 %, 0,9) | |
Note. CRBSI — catheter related blood stream infection.
По результатам парного анализа не выявлено значимых различий при использовании порт-систем в верхней или нижней полой вене в частоте применении урокиназы при дисфункции катетера (р = 0,314), дислокации катетера (р = 0,981), возникновения катетер-ассоциированной инфекции кровотока (р = 0,274), инфекции подкожного кармана (р = 0,075). Различия были выявлены в вероятности возникновения катетер-ассоциированного тромбоза, который при использования бедренного доступа был значимо чаще (р = 0,017), вне зависимости от материала катетера (р = 0,801) (рис. 5). Кроме того, в порт-системах с клапанами на дистальном конце катетера дисфункции возникали чаще, чем в порт-системах с открытым дистальным концом (р = 0,042).
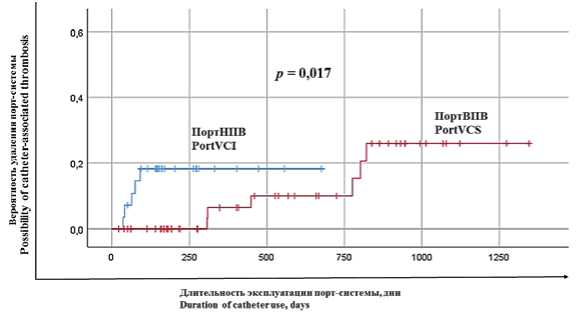
Рисунок 5. Вероятность возникновения катетер-ассоциированных тромбозов при эксплуатации порт-систем (КАТ — катетер-ассоциированный тромбоз, ВПВ — верхняя полая вена, НПВ — нижняя полая вена)
Figure 5. Catheter-associated thrombosis rate in patients with ports (CAT — catheter-associated thrombosis, PortVCS — port in vena cava superior, PortVCI — port in vena cava inferior)
Установлены различия как в общем сроке использования порт-систем в верхней и нижней полых венах (р = 0,0001), так и «бессобытийном» использовании, под которым понимали продолжительность использования порт-систем без каких-либо осложнений (р = 0,002) (рис. 6). Суммарная продолжительность эксплуатации порт-систем, установленных в верхнюю полую вену, составила 31 843 катетеро-дня, в нижнюю полую вену — 6551 катетеро-день.
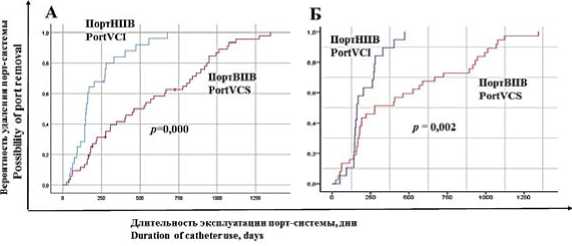
Рисунок 6. Вероятность удаления порт-систем во время эксплуатации, с учетом осложнений (А) и без осложнений (Б)
Figure 6. Figure 6. Port removal rate in patients with (A) and without (Б) complications
Для оценки значения вида катетера на возникновение осложнений сопоставлены результаты использования 35 порт-систем, установленных бедренным доступом, и 156 нетуннелируемых венозных катетеров Certofix Duo 7 Fr, установленных бедренным доступом. Нетуннелируемые катетеры, установленные бедренным доступом, использовали от 1 до 106 дней (медиана — 6 дней), в результате за время лечения больному устанавливали от 1 до 14 нетуннелируемых катетеров. В отличие от этих катетеров порт-системы, установленные бедренным доступом, эксплуатировали в среднем 5 месяцев, а на все лечение у подавляющего большинства больных была достаточна имплантация одной порт-системы (табл. 3)
Таблица 3. Сравнительная характеристика порт-систем и нетуннелируемых катетеров, установленных бедренным доступом
Table 3. Comparison of femoral ports and non-tunnelled femoral catheters
Параметры Parameters | Порт-системы (n = ٣٥) Ports (n = ٣٥) | Нетуннелируемые катетеры (n = ١٥٦) Non-tunneled catheters (n = ١٥٦) |
Количество катетеров у одного больного в период лечения, минимум-максимум (медиана) Number of catheters per patient during treatment, min-max (median) | 1–2 (1) | 1–14 (3) |
Длительность стояния, дни минимум-максимум (медиана) Duration of catheter use, days, min-max (median) | 1–676 (149) | 1–106 (6) |
Катетер-ассоциированный тромбоз, n (%; на 1000 катетеро-дней) Catheter-related thrombosis, n (%, per 1000 catheter days) | 6 (17 %; 0,9) | 16 (10,3 %; 9) |
Катетер-ассоциированная инфекция, n (%; на 1000 катетеро-дней) CRBSI, n (%, per 1000 catheter days) | 2 (5,7 %; 0,3) | 8 (5,1 %; 4,9) |
Note. CRBSI — catheter related blood stream infection.
При использовании нетуннелируемых катетеров выявлено 16 (10,3 %) катетер-ассоциированных тромбозов (инцидентность — 9/1000 катетеро-дней), в отличие от порт-систем, при использовании которых хотя частота тромбозов и была почти в 2 раза выше (17 %), но инцидентность в 10 раз меньше (0,9/1000 катетеро-дней). Более того, лишь у 3 больных при использовании порт-систем тромбозы были клинически значимы, в остальных случаях они протекали бессимптомно и были выявлены лишь при плановом ультразвуковом исследовании. Тромбы протяженностью 2–4 см располагались по ходу бедренной вены от места входа катетера в вену и ни разу не были выявлены в нижней полой вене.
Инцидентность катетер-ассоциированной инфекции кровотока при равной частоте встречаемости была в 16 раз больше при использовании нетуннелируемых катетеров, чем порт-систем, установленных бедренным доступом (табл. 3).
Методом Каплана — Мейера показано, что вероятность возникновения катетер-ассоциированных тромбозов и инфекции кровотока при использовании нетуннелируемых бедренных катетеров значимо больше, чем при использовании порт-систем, установленных бедренным доступом (рис. 7).
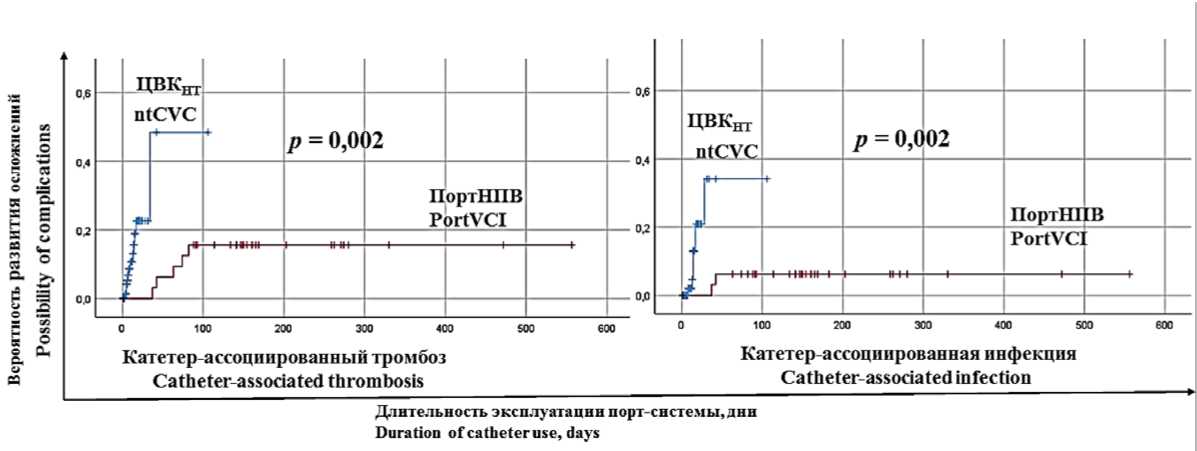
Рисунок 7. Вероятность возникновения катетер-ассоциированных тромбозов и инфекции кровотока при использовании нетуннелируемых бедренных катетеров и порт-систем, установленных бедренным доступом (ЦВКНТ — нетуннелируемый центральный венозный катетер, ПортНПВ — порт-система, установленная в нижнюю полую вену)
Figure 7. Catheter-associated thrombosis and bloodstream infection rates in non-tunnelled femoral catheters and femoral ports (ntCVC — non-tunnelled central venous catheter, PortVCI — port in vena cava inferior)
Обсуждение
Порт-системы нечасто устанавливают бедренным доступом. В разных лечебных учреждениях частота установки порт-систем бедренным доступом варьирует от 0,47 до 3,6 % от всех порт-систем и зависит от контингента больных, проводимого лечения. Особенностью обследованного нами контингента больных явилось включение в исследование только гематологических больных, подавляющее большинство из которых составили больные лимфомами. Эти данные отличаются от результатов N. Wolosker и соавт. [8], согласно которым в установке порт-систем бедренным доступом нуждались в 90 % случаев больные солидными опухолями и лишь в 10 % — онкогематологические больные. Среди онкогематологических больных синдром верхней полой вены — нередкое осложнение: он выявляется у 13,1 % больных лимфомами в целом и у 60 % больных первичной медиастинальной В-крупноклеточной лимфомой в частности [7].
При установке порт-системы бедренным доступом одним из вопросов, которые приходится решать, является локализация камеры порт-системы. Камеру порт-системы при этом доступе можно расположить на грудной клетке, на передней брюшной стенке или на бедре (рис. 8).
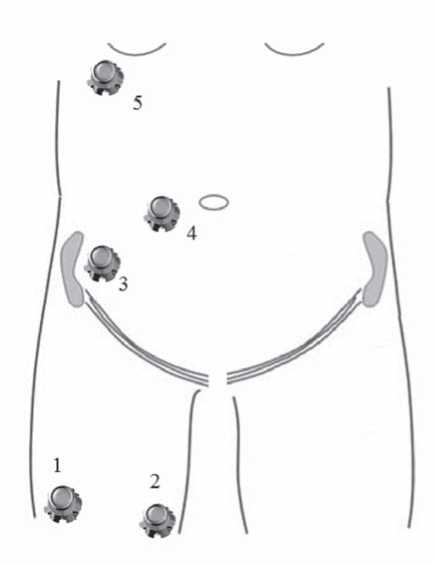
Рисунок 8. Различные локализации камеры при установке порт-системы бедренным доступом. 1 — на латеральной поверхности бедра, 2 — на медиальной поверхности бедра, 3 — на остью подвздошной кости, 4 — треть расстояния от пупка до передней подвздошной ости, 5 — на передней поверхности грудной клетки
Figure 8. Possible localities for femoral port cameras. 1 — lateral proximal third of thigh, 2 — medial proximal third of thigh, 3 — above anterior superior iliac spines, 4 — one-third distance from umbilicus to anterior superior iliac spine, 5 — anterior thoracic wall
Ни одна из локализаций камеры не влияла на физическую активность больных [11][19]. Расположение на грудной стенке камеры порт-системы, установленной бедренным доступом, приводит к значительному удлинению подкожного канала и катетера, что повышает риск его тромботической окклюзии. При расположении камеры на животе из-за избыточной жировой клетчатки могут возникнуть сложности с пункцией и необходимости использовать только длинные иглы Губера, а из-за боли во время пункции происходит сокращение мышц живота, что затрудняет установку иглы в камере [19]. В клиническом наблюдении из Индии [22] сообщается о 56-летней женщине с метастатической карциномой груди и частичным тромбозом верхней полой вены. Ей была установлена порт-система через бедренную вену, а резервуар помещен на живот, справа ниже пупка. Это привело к возникновению сразу двух осложнений: во-первых, из-за ожирения невозможно было пальпировать резервуар и приходилось при пункции пользоваться ультразвуковой навигацией, а во-вторых, из-за глубокого расположения резервуара и большой толщины подкожно-жировой клетчатки длины иглы Губера было недостаточно и для пункции использовали спинальную иглу. Расположение камеры на бедре позволяет поместить ее на твердую костную основу, при этом используется наименьшая длина катетера, что уменьшает риск его окклюзии, здесь меньше подкожный жировой слой, фасция близко расположена к коже, кроме того больные могут легко пунктировать порт-систему самостоятельно, а сама пункция менее болезненна. Если пациент предпочитает спать на боку, то камера может быть помещена не латерально, а медиально. Опрос, проведенный среди медицинского персонала и больных, показал, что большинство из них предпочло локализацию резервуара порт-системы на бедре [13].
Для того чтобы определить преимущества и недостатки порт-систем, установленных бедренным доступом, их сравнили с порт-системами, установленными в верхнюю полую вену, что позволило оценить, как влияет разная локализация одного и того же сосудистого устройства на развитие осложнений. В настоящем исследовании частота возникновения катетер-ассоциированной инфекции кровотока и инфекции подкожного кармана значимо не различалась при обеих локализациях, однако инцидентность этих осложнений была в 3–4 раза больше при бедренном доступе (соответственно 0,3/1000 и 0,4/1000 катетеро-дней против 0,13/1000 и 0,1/1000 катетеро-дней). Это означает, что эти осложнения возникали при более коротком периоде использования порт-систем, установленных бедренным доступом. По данным других авторов, использовавших порт-системы, установленные бедренным доступом, катетер-ассоциированная инфекция кровотока встречалась в 10–21 % случаев (инцидентность — 0,46/1000 катетеро-дней), а инфекция кармана — в 5,6 % (0,23/1000 — 0,5/1000 катетеро-дней) [8][10][12], т. е. даже чаще, чем в настоящем исследовании, в котором все онкогематологические больные получали противоопухолевую химиотерапию, после которой у большинства из них развивалась выраженная нейтропения.
Другим значимым осложнением явились катетер-ассоциированные тромбозы, которые встречались чаще при использовании порт-систем, установленных в нижнюю, чем в верхнюю полую вену (8,3 % против 17 %, р = 0,017), больше была и инцидентность — 0,9/1000 против 0,2/1000 катетеро-дней. В нашем исследовании тромбозы выявлялись чаще, чем в работах других авторов, согласно которым частота тромбоза глубоких вен колебалась от 5 до 19 %, а инцидентность составила 0,23/1000 катетеро-дней [8][10]. Возможным объяснением является тот факт, что в нашем исследовании у всех больных после катетеризации регулярно проводилось ультразвуковое исследование вен, у большинства из них тромбозы протекали бессимптомно.
С другой стороны, возникает вопрос: надо ли устанавливать порт-систему в бедренную вену или проще катетеризировать бедренную вену нетуннелируемым катетером? Но нетуннелируемые катетеры в бедренной вене не предусмотрены для длительного и тем более амбулаторного использования. Следовательно, они должны устанавливаться перед каждым очередным курсом химиотерапии и удаляться перед выпиской больного из стационара. В результате медиана продолжительности использования таких катетеров составляла 6 дней, а за время лечения лимфомы больному приходилось устанавливать от 1 до 14 (медиана — 3) нетуннелируемых венозных катетеров, установленных бедренным доступом. В то же время было достаточно одной порт-системы на все время лечения, и медиана продолжительности ее эксплуатации — 149 дней. Но дело даже не в количестве установленных катетеров, хотя каждая катетеризация вены чревата осложнениями. В 5,3 % случаев, по некоторым данным, вообще не удавалось катетеризировать бедренную вену [23]. Применение ультразвуковой навигации чаще позволяет катетеризировать бедренную вену с первой попытки [24]. В нашем исследовании все катетеризации выполнялись только под ультразвуковым контролем, и не было осложнений, обусловленных пункцией вены. Имелись различия в частоте осложнений в процессе эксплуатации сосудистого доступа. Частота катетер-ассоциированных тромбозов при катетеризации нетуннелируемыми катетерами в нашем исследовании составила 10,3 %, что больше, чем в исследовании J-J. Parienti и соавт. [23], в котором при 844 катетеризациях бедренных вен частота симптоматических тромбозов составила 1,4 %, при этом катетеры использовались, как и в нашем исследовании, в среднем 5,9 дня. Столь значительные различия можно объяснить, во-первых, частыми повторными катетеризациями одной и той же вены, что повышает риск тромботических осложнений, а во-вторых, тем, что в нашем исследовании выявляли не только симптоматические, но и бессимптомные тромбозы, поскольку при использовании бедренного доступа регулярно выполнялось ультразвуковое исследование как по мере эксплуатации катетера, так и перед каждой последующей катетеризацией. Этим же можно объяснить и большую частоту тромбозов (17 %), выявляемых при использовании порт-систем, тем более что большинство из них были бессимптомными и являлись находкой при ультразвуковом исследовании. При этом все равно инцидентность катетер-ассоциированных тромбозов была в 10 раз была меньше при использовании порт-систем по сравнению с нетуннелируемыми катетерами (0,9/1000 против 9/1000 катетеро-дней) и меньше, чем в исследовании других авторов (4,6/1000 катетеро-дней) [23].
Другой проблемой при использовании бедренного доступа была катетер-ассоциированная инфекция. Частота инфекционных осложнений была одинаковой при использовании порт-систем и нетуннелируемых катетеров (соответственно 5,7 и 5,1 %). Она больше, чем при использовании венозного бедренного катетера в других исследованиях (1,2–1,44 %) [23][25], но в нашем исследовании катетеры устанавливались иммунокомпрометированным больным, получавшим химиотерапию, после которой у большинства развивалась нейтропения. Несмотря на это, инцидентность инфекции кровотока при использовании порт-систем, установленных бедренным доступом (0,3/1000 катетеро-дней), оказалась значительно меньше, чем при использовании нетуннелируемых катетеров (4,9/1000 катетеро-дней).
Таким образом, при использовании порт-систем, установленных бедренным доступом, по сравнению с порт-системами, установленными в верхнюю полую вену, чаще возникают осложнения. Однако установка порт-системы через бедренную вену — это вынужденная мера в безвыходной ситуации, когда нет доступа через сосуды бассейна верхней полой вены [19]. При этом порт-система, установленная бедренным доступом, имеет целый ряд преимуществ как по частоте катетеризаций, так и по инцидентности инфекционных и тромботических осложнений по сравнению с нетуннелируемыми катетерами, установленными бедренным доступом. В случае восстановления проходимости верхней полой вены бедренный порт может быть заменен на другой катетер в верхней полой вене либо, если нет осложнений, через него может быть продолжено лечение.
Список литературы
1. Gow K.W., Tapper D., Hickman R.O. Between the lines: The 50th anniversary of long-term central venous catheters. Am J Surg. 2017; 213(5): 837–48. DOI: 10.1016/j.amjsurg.2017.03.021.
2. Niederhuber J.E., Ensminger W., Gyves J.W. et al. Totally implanted venous and arterial access system to replace external catheters in cancer treatment. Surgery. 1982; 92(4): 706–12.
3. Kim D., Ryu D., Jung H. et al. Evaluation of complications of totally implantable central venous port system insertion. Exp Ther Med. 2019; 17(3): 2013–8. DOI: 10.3892/etm.2019.7185.
4. Wu O., Boyd K., Paul J. et al. Hickman catheter and implantable port devices for the delivery of chemotherapy: A phase II randomised controlled trial and economic evaluation. Br J Cancer. 2016; 114(9): 979–85. DOI: 10.1038/bjc.2016.76.
5. Fang S., Yang J., Song L. et al. Comparison of three types of central venous catheters in patients with malignant tumor receiving chemotherapy. Patient Prefer Adherence. 2017; 11: 1197–204. DOI: 10.2147/PPA.S142556.
6. Ng F., Mastoroudes H., Paul E. et al. A comparison of Hickman line- and Port-aCath-associated complications in patients with solid tumours undergoing chemotherapy. Clin Oncol. 2007; 19(7): 551–6. DOI: 10.1016/j.clon.2007.04.003.
7. Галстян Г.М., Спирин М.В., Терехова И.В. и др. Особенности обеспечения центрального венозного доступа у больных лимфомами. Анестезиология и реаниматология. 2018; 63(2): 119–26.
8. Wolosker N., Yazbek G., Munia M.A. et al. Totally implantable femoral vein catheters in cancer patients. Eur J Surg Oncol. 2004; 30(7): 771–5. DOI: 10.1016/j.ejso.2004.05.019.
9. Harish K., Madhu Y.C. Femoral Port Placement — Report of Two Cases. Indian J Surg Oncol. 2011; 2(1): 31–3. DOI: 10.1007/s13193-011-0071-9.
10. Almasi-Sperling V., Hieber S., Lermann J. et al. Femoral placement of totally implantable venous access ports in patients with bilateral breast cancer. Geburtshilfe Frauenheilkd. 2016; 76(1): 53–8. DOI: 10.1055/s-0035-1558173.
11. Chen S.-Y., Lin C.H., Chang H.-M. et al. A safe and effective method to implant a totally implantable access port in patients with synchronous bilateral mastectomies: Modified femoral vein approach. J Surg Oncol. 2008; 98(3): 197–9. DOI: 10.1002/jso.21048.
12. Goltz J.P., Janssen H., Petritsch B. et al. Femoral placement of totally implantable venous power ports as an alternative implantation site for patients with central vein occlusions. Support Care Cancer. 2014; 22(2): 383–7. DOI: 10.1007/s00520-013-1984-3.
13. Heiss P., Stroszczynski C., Gössmann H. Okklusion der V. cava superior. Radiologische implantation eines zentralvenösen portsystems über einen femoralen zugang. Radiologe. 2012; 52(5): 455–8. DOI: 10.1007/s00117-012-2317-0.
14. Dholaria S., Yadav D., Gupta A. Chemo port insertion through femoral vein approach: A rare indication and a rare complication. Indian J Cancer. 2017; 54(1): 361. DOI: 10.4103/ijc.ijc_193_17.
15. Meyer F., Buerger T., Gebauer T. et al. Unusual implantation site of a port-acath system via the right femoral vein. J Cancer Res Clin Oncol. 2002; 128(7): 400–1. DOI: 10.1007/s00432-002-0353-2.
16. Дубовик П.Л., Хлебников Б.А., Шайдоров М.В. Имплантируемые инфузионные порт-системы в онкологии. Тольяттинский медицинский консилиум. 2011; (5–6): 55–60.
17. Добыш К.Н., Глушанина А.C. Имплантируемая порт-система для центрального венозного доступа в лечении туберкулеза с множественной / широкой лекарственной устойчивостью. Актуальные проблемы современной медицины и фармации — 2017: сборник тезисов докладов LXXI Междунар. научно-практ. конф. студентов и молодых ученых. Минск, 17–19 апр. 2017 г. Минск: БГМУ, 2017; 125–8.
18. Cherkashin M., Berezina N., Puchkov D. et al. Femoral access for central venous port system implantation. Cureus. 2018; 10(3): 3–6. DOI: 10.7759/cureus.2327.
19. Toro A., Mannino M., Cappello G. et al. Totally implanted venous access devices implanted in the saphenous vein. Relation between the reservoir site and comfort / discomfort of the patients. Ann Vasc Surg. 2012; 26(8): 1127.e9–13. DOI: 10.1016/j.avsg.2012.02.025.
20. Sharp R., Cummings M., Fielder A. et al. The catheter to vein ratio and rates of symptomatic venous thromboembolism in patients with a peripherally inserted central catheter (PICC): A prospective cohort study. Int J Nurs Stud. 2015; 52(3): 677–85. DOI: 10.1016/j.ijnurstu.2014.12.002.
21. Seldinger S.I.S.I. Catheter replacement of the needle in percutaneous arteriography; a new technique. Acta radiol. 1953; 39(5): 368–76. DOI: 10.3109/00016925309136722.
22. Nosocomial infection rates for interhospital comparison: limitations and possible solutions. Infect Control Hosp Epidemiol. 1991; 12(10): 609–21. DOI: 10.1086/646250.
23. Parienti J.J., Mongardon N., Mégarbane B. et al. Intravascular complications of central venous catheterization by insertion site. N Engl J Med. 2015; 373(13): 1220–9. DOI: 10.1056/NEJMoa1500964.
24. Brass P., Hellmich M., Kolodziej L. et al. Ultrasound guidance versus anatomical landmarks for subclavian or femoral vein catheterization. Cochrane Database Syst Rev. 2015; 1(1). DOI: 10.1002/14651858.CD011447. www.cochranelibrary.com.
25. Deshpande K.S., Hatem C., Ulrich H.L. et al. The incidence of infectious complications of central venous catheters at the subclavian, internal jugular, and femoral sites in an intensive care unit population. Crit Care Med. 2005; 33(1): 13–20. DOI: 10.1097/01.CCM.0000149838.47048.60.
Об авторах
Г. М. ГалстянРоссия
Галстян Геннадий Мартинович, доктор медицинских наук, заведующий отделением реанимации и интенсивной терапии
125167, Москва
М. В. Спирин
Россия
Спирин Михаил Васильевич, кандидат медицинских наук, врач отделения реанимации и интенсивной терапии
125167, Москва
М. Ю. Дроков
Россия
Дроков Михаил Юрьевич, кандидат медицинских наук, руководитель сектора по изучению иммунных воздействий и осложнений после ТКМ
125167, Москва
И. Э. Костина
Россия
Костина Ирина Эдуардовна, кандидат медицинских наук, заведующая отделением рентгенодиагностики и компьютерной томографии
125167, Москва
Я. К. Мангасарова
Россия
Мангасарова Яна Константиновна, кандидат медицинских наук, заведующая дневным стационаром отделения высокодозной химиотерапии
125167, Москва
Рецензия
Для цитирования:
Галстян Г.М., Спирин М.В., Дроков М.Ю., Костина И.Э., Мангасарова Я.К. Преимущества и недостатки порт-систем, установленных бедренным доступом, у гематологических больных с синдромом верхней полой вены. Гематология и трансфузиология. 2020;65(4):403-416. https://doi.org/10.35754/0234-5730-2020-65-4-403-416
For citation:
Galstyan G.M., Spirin M.V., Drokov M.Yu., Kostina I.E., Mangasarova Ya.K. Advantages and disadvantages of femoral port systems in hematоlogical patients with superior vena cava syndrome. Russian journal of hematology and transfusiology. 2020;65(4):403-416. (In Russ.) https://doi.org/10.35754/0234-5730-2020-65-4-403-416











































