Перейти к:
Крупноклеточная В-клеточная лимфома с перестройкой IRF4
https://doi.org/10.35754/0234-5730-2021-66-3-445-457
Аннотация
Введение. Крупноклеточная В-клеточная лимфома с перестройкой IRF4 — редкая патология, возникает у детей и молодых взрослых, протекает с вовлечением лимфатических узлов головы, шеи и/или лимфоидного кольца Пирогова — Вальдейера. Особенностью опухоли является экспрессия белка MUM1 c перестройкой гена IRF4/6p25.3.
Цель — представить клиническое наблюдение крупноклеточной В-клеточной лимфомы с перестройкой IRF4.
Основные данные. Представлено наблюдение за больным IRF4-позитивной крупноклеточной В-клеточной лимфомой. Диагноз установлен на основании морфологического, иммуногистохимического, цитогенетического исследований, флуоресцентной гибридизации in situ и клинических проявлений. Особенностью случая явился преимущественно диффузный характер роста крупных опухолевых клеток в биоптате лимфатического узла в сочетании с индолентным клиническим течением заболевания, а также наличие цитогенетических аберраций обоих гомологов хромосомы 6: перестройки IRF4 и делеции 6p25. Проведение четырех курсов R-CHOP-21 позволило достичь ремиссии заболевания, сохраняющейся в течение 26 мес.
Ключевые слова
Для цитирования:
Пластинина Л.В., Моисеева Т.Н., Аль-Ради Л.С., Ковригина А.М., Обухова Т.Н., Горячева С.Р., Шуплецова И.А., Магомедова А.У., Кравченко С.К. Крупноклеточная В-клеточная лимфома с перестройкой IRF4. Гематология и трансфузиология. 2021;66(3):445-457. https://doi.org/10.35754/0234-5730-2021-66-3-445-457
For citation:
Plastinina L.V., Moiseeva T.N., Al-Radi L.S., Kovrigina A.M., Obukhova T.N., Goryacheva S.R., Shupletsova I.A., Magomedova A.U., Kravchenko S.K. Large B-cell lymphoma with IRF4 rearrangement. Russian journal of hematology and transfusiology. 2021;66(3):445-457. (In Russ.) https://doi.org/10.35754/0234-5730-2021-66-3-445-457
Введение
Крупноклеточная В-клеточная лимфома с перестройкой IRF4 (interferon regulatory factor 4 — интерферон-регуляторный фактор 4)(IRF4-позитивная лимфома), сочетающая признаки фолликулярной лимфомы (ФЛ) 3-го цитологического типа и диффузной В-клеточной крупноклеточной лимфомы (ДВККЛ), предложена в качестве отдельной нозологической формы в классификации ВОЗ [1]. При сходстве морфологических признаков ФЛ и ДВККЛ данная лимфома не относится к вариантам ФЛ или ДВККЛ, поскольку имеет характерную цитогенетическую аномалию — перестройку локуса гена IRF4/6 р25, а также ряд клинических и лабораторных особенностей. Ген IRF4 принадлежит к семейству регуляторных факторов интерферона. Данное семейство включает группу из 10 транскрипционных факторов, участвующих в регуляции генов в ответ на действие интерферонов [2]. IRF4 первоначально описан как лимфоцит-специфичный регуляторный фактор интерферона (LSIRF — lymphocyte-specific interferon regulatory factor) — сигнальная молекула, обнаруженная в селезенке мыши [3]. Его человеческий гомолог — human LSIRF — впоследствии был переименован в IRF4 [4]. Ген IRF4 расположен на коротком плече 6-й хромосомы локусе 25.3. В норме IRF4 кодирует экспрессию белка MUM1 (multiple myeloma oncogene-1 — онкоген множественной миеломы (ММ) 1). S. Iida и соавт. [4] идентифицировали ген IRF4 как участника транслокации t(6;14)(p25;q32) при ММ, однако ассоциации данной перестройки с клиническим течением заболевания или экспрессией белка MUM1 при ММ не наблюдается [5], т. е. перестройка IRF4 не является единственным механизмом активации экспрессии белка MUM1. In vitro IRF4 обладает онкогенной активностью [6], однако активации этого гена недостаточно для развития лимфоидной опухоли, что было показано в экспериментах на трансгенных мышах [7]. Одним из продуктов активации гена IRF4 является белок MUM1 — ключевой регулятор нескольких этапов дифференцировки лимфоидных, миелоидных и дендритных клеток. MUM1 играет важную роль в активации лимфоцитов и терминальной В-клеточной дифференцировке. В отличие от других участников семейства IRF, MUM1 нечувствителен к действию интерферонов, но его активность может изменяться под воздействием таких стимулов, как конкавалин А, стафилококковый энтеротоксин А, интерлейкин 4, липополисахариды, CD40 — известных как индукторы дифференцировки и активации лимфоцитов через активацию NFKB (nuclear factor kappa-light-chain-enhancer of activated B cells — ядерный фактор легкой цепи каппа активированных В-клеток) [7–9]. В физиологических условиях белок MUM1 экспрессируется в ядрах и цитоплазме плазматических клеток, небольшого числа В-лимфоцитов «светлых зон» герминального центра, и в активированных Т-клетках [10]; может определяться в меланоцитах кожи [3]. В экспериментах у IRF4-дефицитных мышей отсутствуют герминальные центры фолликулов в лимфатических узлах, отсутствуют плазматические клетки и наблюдается глубокая гипогаммаглобулинемия [4][6]. В физиологических условиях MUM1-позитивные В-клетки не экспрессируют белок BCL6. Таким образом, MUM1 является маркером перехода В-клеток от BCL6-позитивных В-клеток герминального центра к постгерминальной/плазмоклеточной дифференцировке [11].
Экспрессия MUM1 характерна для многих гематологических опухолей. В зависимости от частоты встречаемости экспрессии MUM1 в опухолевых клетках выделяют две группы лимфом. Лимфоидные опухоли, в которых большинство опухолевых клеток и почти во всех наблюдениях экспрессируют MUM1, — это ММ, классическая лимфома Ходжкина, ДВККЛ non-GCB типа, анапластическая крупноклеточная лимфома; лимфомы с вариабельной частотой экспрессии MUM1 включают лимфоцитарную лимфому/В-хронический лимфолейкоз, лимфому Беркитта, лимфому из клеток зоны мантии, периферические Т-клеточные лимфомы [12]. Экспрессия MUM1 обусловливает прогностически неблагоприятный non-GCB иммуногистохимический подтип ДВККЛ, ассоциирована с худшим прогнозом при лимфоме Беркитта [13]. При классическом варианте лимфомы Ходжкина отсутствие экспрессии MUM1 ассоциировалось с неблагоприятным прогнозом, уменьшением общей выживаемости и времени до прогрессирования [14]. При ФЛ экспрессия MUM1 ассоциирована с 3-м цитологическим типом, высоким индексом пролиферативной активности Ki-67, худшими исходами заболевания [15], а также с ранней трансформацией ФЛ в ДВККЛ [16].
Наиболее чувствительным методом определения перестройки IRF4 является флуоресцентная гибридизация in situ (fluorescence hybridization in situ — FISH). Партнером по перестройке IRF4 в 85 % случаев является локус генов тяжелых цепей иммуноглобулинов (IGH), располагающийся на хромосоме 14. Редко в этом качестве выступают локусы генов легких цепей иммуноглобулинов, расположенные на хромосомах 2 (IGK) и 22 (IGL), или другие локусы неизвестных генов [17]. Остается неясным клиническое значение хромосомного партнера, участвующего в транслокации IRF4. Описаны три случая выявления перестройки IRF4 у взрослых больных индолентными мелкоклеточными В-клеточными лимфомами, во всех случаях хромосомными партнерами являлись не IGH-локусы: в 2 случаях — IGL и IGK, в одном случае партнер не установлен [18]. Один из случаев c перестройкой IGK [17] являлся трансформированной В-клеточной лимфомой, из чего делают вывод, что перестройка IRF4 встречается не только при агрессивных лимфомах, но и при индолентных лимфомах, и, возможно, связана с трансформацией индолентного заболевания.
Транслокация IGH/IRF4 при В-клеточных лимфомах впервые описана в 2001 г. Akiko Tamura у одного из 173 обследованных больных — молодого мужчины 17 лет [19]. В 2010 г. K. E. Hunt и соавт. предположили, что генетической основой экспрессии белка MUM1 при ДВККЛ является перестройка гена IRF4. Однако она выявлена только у одного из 15 больных non-GCB вариантом ДВККЛ [20]. В поиске новых партнеров по транслокации IGH у больных В-клеточными лимфомами (ДВККЛ и ФЛ 3-го цитологического типа) I. Salaverria и соавт. идентифицировали неоднократно повторяющийся перестроенный локус гена IRF4, который совместно с IGH, IGL, IGK и неизвестными партнерами выявлен у 20 из 427 больных. Вероятность возникновения лимфомы уменьшалась с возрастом, болели преимущественно дети и молодые взрослые (медиана возраста — 12 лет) [17].
Уровень транскрипта IRF4 статистически значимо выше при IRF4-позитивной лимфоме, чем при АВС — молекулярном подтипе ДВККЛ, а BCL6 выше, чем при GCB подтипе ДВККЛ. По сравнению с IRF4-негативными случаями (n = 136), лимфомы с перестройкой IRF4 (n = 7) показали отличающийся профиль экспрессии по 132 генам: 123 гена с повышенной и 9 — с пониженной экспрессией в IRF4-позитивных случаях. На основе профиля экспрессии генов авторы создали схему, где выделили 27 генов, по которым с вероятностью 96 % можно предсказать наличие перестройки IRF4 при В-клеточной лимфоме. Это исследование проводилось в разнородной по возрасту группе больных. При исследовании однородной группы больных в возрасте до 25 лет также было показано, что лимфома с перестройкой IRF4 имеет свой уникальный молекулярно-генетический профиль. Помимо транслокации IRF4 встречались частые мутации генов NFKB — сигнального пути, в отличие от ДВККЛ той же возрастной категории молодых больных (18–25 лет) [21].
Показано, что 95 % больных IRF4-позитивной лимфомой имеют дополнительные хромосомные нарушения. Лица моложе и старше 18 лет имеют примерно одинаковое число хромосомных аберраций в кариотипе (около 6 на случай). Такие же результаты получены при сравнении у лиц моложе и старше 40 лет [22]. Перестройка IRF4 часто сочетается с аберрациями BCL6 [17]. Сочетания с перестройкой гена BCL2 не описаны. Наиболее частыми хромосомными нарушениями являются амплификации Хq28, 11q22.3-qter, 7q32.1-qter, делеции 6q13–16.1, 15q14–22.31 и 17р. Нарушения хромосомы 17 выявлены у 22 % больных [22]. Клинические данные и результаты лечения больных с аберрациями 17-й хромосомы в настоящее время не описаны.
Таким образом, IRF4-позитивная лимфома встречается в 0,05 % случаев при ДВККЛ/ФЛ 3-го цитологического типа [17], в 8 % — при ДВККЛ с вовлечением миндалин [23], в 50 % — при вовлечении миндалин с экспрессией опухолевыми клетками MUM1 при ФЛ у детей [24]. Возраст больных — от 4 до 79 лет, медиана — 12 лет. В трети случаев заболевание встречается у взрослых больных. В отличие от ФЛ педиатрического типа (ФЛПТ), при которой чаще заболевают лица мужского пола, при данной лимфоме нет гендерных различий. Клинически заболевание характеризуется локальными стадиями (I–II стадии по Ann Arbor [25]) с вовлечением лимфатических узлов головы, шеи и/или лимфоидного кольца Пирогова — Вальдейера. Описан случай IRF4-позитивной лимфомы с вовлечением миндалин у мальчика 8 лет, протекавшей с эпизодами ночного апноэ [26], а также случаи с вовлечением лимфатических узлов ниже диафрагмы, желудочно-кишечного тракта, обнаружением опухолевых клеток в спинномозговой жидкости [26][27].
Нормальным неопухолевым аналогом клеток IRF4-позитивной лимфомы являются В-лимфоциты герминального центра. В норме на поздних этапах герминальной дифференцировки В-лимфоцитов увеличение экспрессии MUM1 подавляет экспрессию BCL6 и активирует BLIMP1, приводя к переходу В-лимфоцита на этап плазмоцитарной дифференцировки. В данной опухоли отмечается коэкспрессия белков МUM1 и BCL6 в сочетании с недостаточной экспрессией BLIMP1. Экспрессия MUM1 выявляется в 100 % случаев, BCL6 — в 94–100 %, позитивность по BCL-2 и CD10 встречается в 65 % наблюдений. Индекс пролиферативной активности Ki-67 — высокий [17]. Опухоль не подлежит оценке по иммуногистохимическому алгоритму Hans для ДВККЛ [28].
Дифференциальную диагностику IRF4-позитивной лимфомы проводят с реактивной фолликулярной гиперплазией. Наличие аберрантного иммунофенотипа с коэкспрессией MUM1, BCL6 и часто экспрессией CD10, наличие клональной перестройки генов тяжелой цепи иммуноглобулина, а также перестройки IRF4 позволяют установить диагноз. Дифференциальную диагностику проводят с ФЛПТ, поскольку оба процесса сходны по локализации и возрасту больных, а также гистологической картине опухоли. В отличие от ФЛПТ, при IRF4-позитивной лимфоме митозы встречаются нечасто, а картина «звездного неба» отсутствует. Яркая экспрессия MUM1 позволяет заподозрить, а наличие перестройки IRF4 подтвердить диагноз IRF4-позитивной лимфомы. I–II стадия заболевания с вовлечением шейных лимфатических узлов и/или кольца Пирогова — Вальдейера у молодых больных в сочетании с морфологической картиной крупноклеточной лимфомы не всегда указывают на IRF4-позитивную лимфому или ФЛПТ. Спектр дифференциальной диагностики лимфом включает также ДВККЛ NOS (not otherwise specified), ФЛ 3-го цитологического типа, В-клеточную лимфому высокой степени злокачественности, лимфому Беркитта. Дифференциальная диагностика основывается на выявлении комплекса гистологических, иммунофенотипических и цитогенетических особенностей. Три критерия могут указывать на наличие IRF4-позитивной лимфомы: молодой возраст, локализация в области лимфатических узлов головы и шеи и/или лимфоидного кольца Пирогова — Вальдейера и иммуногистохимический профиль, включающий экспрессию опухолевыми клетками MUM1 и BCL6, в ряде случаев — в сочетании с CD10. Предлагается у всех больных с подходящими клиническими, морфологическими и иммуногистохимическими критериями исследовать перестройку IRF4 [27].
Нет общепринятых рекомендаций по лечению IRF4-позитивной лимфомы. Лечение осуществляют по интенсивным или неинтенсивным химиотерапевтическим программам. Прогноз у больных, получающих химиотерапевтическое лечение с лучевой терапией или без лучевой терапии, благоприятный [17]: 5-летняя общая выживаемость составила 100 %, что больше, чем при ДВККЛ/ФЛ 3-го цитологического типа без перестройки IRF4 (период наблюдения — 1–191 мес., медиана — 105 мес.). Однако при разделении больных лимфомами без перестройки IRF4 в зависимости от возраста (моложе или старше 60 лет), различия в выживаемости в группе молодых больных по сравнению с больными IRF4-позитивной лимфой были незначимы. По рекомендациям NCCN [29], взрослых больных В-клеточной лимфомой с перестройкой IRF4 следует лечить по программам для ДВККЛ, при локальных стадиях болезни — по программе «R-CHOP» для обоих вариантов лимфом. Имеются описания единичных клинических случаев IRF4-позитивной лимфомы с вовлечением миндалин у детей, которым проводили только тонзилэктомию без системной химиотерапии, в дальнейшем в течение 2 лет у них не было признаков болезни [24][30]. Имеет ли значение возраст пациентов и локализация опухолевого процесса (только миндалины, или только лимфатические узлы) с точки зрения дальнейшего течения заболевания после хирургического удаления опухоли в настоящее время неизвестно. У 3 больных детского возраста (6 лет, 6 лет и 2,7 года) после удаления миндалин при наличии увеличенных шейных лимфатических узлов проводили 2 курса редуцированной химиотерапии по программе COPAD. Ремиссия сохранялась у всех детей в течение 8, 15 и 15 мес. [31].
Описано наблюдение резистентной к терапии R-CHOP IRF4-позитивной лимфомы у мужчины 52 лет, страдавшего также парциальной красноклеточной аплазией (ПККА) тяжелой степени, леченой химиотерапией и гормонотерапией, и развившейся за 2 года до дебюта лимфомы [32]. Партнером по перестройке IRF4 явилась 2-я хромосома, присутствовали дополнительные нарушения кариотипа (add(5)(p15)). Терапия R-CHOP позволила достичь частичной ремиссии, сохранявшейся в течение 10 мес. ПККА прогрессировала, несмотря на лечение ритуксимабом. В фазе прогрессии заболевания, помимо транслокации с участием гена IRF4 — t(2;6)(p11.2; p25), в опухолевых клетках костного мозга выявлена делеция локуса гена CDKN2A/2B, что, возможно, являлось причиной резистентности заболевания. Таким образом, прогностическое значение обнаружения перестройки IRF4 при В-клеточных лимфомах противоречиво. Имеющиеся в литературе данные представлены в таблице 1.
Таблица 1. Крупноклеточная В-клеточная лимфома с перестройкой IRF4
Table 1. Large-cell B-cell lymphoma with IRF4 rearrangement
|
№ |
Ссылка Reference |
Число больных Number of patients |
Возраст больных (лет) Age (years) |
Локализация Localization |
Лечение Treatment |
Результат лечения Treatment results |
Период наблюдения (мес.) Observation period (months) |
|
Крупноклеточные В-клеточные лимфомы с перестройкой IRF4 Large-cell B-cell lymphoma with IRF4 rearrangement |
|||||||
|
1 |
[17] |
20 |
4–79 (медиана — 12 лет) 4–79 (Me — 12 y. o.) |
Преимущественно лимфоузлы головы и шеи с вовлечением кольца Пирогова — Вальдейера Mainly lymph nodes head and neck with Pirogov — Waldeyer ring involvement |
ХТ CT |
5-ОВ = 100 % 5-OS = 100 % |
|
|
2 |
[23] |
2 |
32 |
Миндалины Tonsils |
CHOP+ЛТ; CHOP+RT |
ПР CR |
н/д unknown |
|
79 |
Миндалины Tonsils |
ХТ с антрациклинами CT with anthracyclines |
ПР CR |
н/д unknown |
|||
|
3 |
[24] |
3 |
3 |
Миндалины Tonsils |
ЦД СD |
ПР CR |
62 |
|
15 |
Миндалины Tonsils |
н/д unknown |
н/д unknown |
н/д unknown |
|||
|
18 |
Миндалины Tonsils |
н/д unknown |
н/д unknown |
н/д unknown |
|||
|
4 |
[32] |
1 |
52 |
Генерализованная лимфаденопатия Generalized lymphadenopathy |
R-CHOP № 4 R-CHOP No. 4 |
ЧР PR |
прогрессия через 10 мес. progression after 10 months |
|
5 |
[30] |
2 |
5 |
Миндалины Tonsils |
Тонзиллэктомия; Tonsillectomy |
ПР CR |
24 |
|
22 |
Миндалины Tonsils |
Тонзиллэктомия+R-CHOP № 3+ЛТ Tonsillectomy+R-CHOP No. 3+RT |
ПР CR |
н/д unknown |
|||
|
6 |
[27] |
1 |
12 |
Паховый лимфоузел слева Left inguinal lymph node |
ХТ CT |
ПР CR |
н/д unknown |
|
7 |
[33] |
1 |
19 |
Миндалины Tonsils |
Тонзиллэктомия+R-CHOP № 6 Tonsillectomy+R-CHOP No. 6 |
ПР CR |
26 |
|
8 |
[31] |
4 |
8 |
Миндалины Tonsils |
Тонзиллэктомия+NHL BFM90 № 4 Tonsillectomy+NHL BFM90 No. 4 |
ПР CR |
55 |
|
6 |
Миндалины Tonsils |
Тонзиллэктомия+COPAD № 2 Tonsillectomy+COPAD No. 2 |
ПР CR |
15 |
|||
|
2.7 |
Миндалины Tonsils |
Тонзиллэктомия+COPAD № 2; Tonsillectomy+COPAD No. 2 |
ПР CR |
15 |
|||
|
6 |
Миндалины Tonsils |
Тонзиллэктомия+COPAD № 2 Tonsillectomy+COPAD No. 2 |
ПР CR |
8 |
|||
|
9 |
[26] |
2 |
5,9 |
Миндалины+ликвор; Tonsils+cerebrospinal fluid |
ХТ (CHOE+MTX+AraC) +интратекально mtx+АraC СT (CHOE+MTX+AraC) +intrathecal mtx+АraC |
ПР CR |
45 |
|
16,3 |
Илеоцекальный угол кишки Intestine ileocecal angle |
ХТ CT |
ПР CR |
48 |
|||
|
10 |
[34] |
1 |
8 |
Миндалины Tonsils |
тонзиллэктомия tonsillectomy |
ПР CR |
н/д unknown |
|
11 |
[35] |
15 |
< 60 лет (n = 10) > 60 лет (n = 5) < 60 y. o. (n = 10) > 60 y. o. (n = 5) |
Стадия по Ann Arbor: I/II (n = 3), III/IV без костного мозга (n = 12) Stage by Ann Arbor: I/II (n = 3), III/IV without bone marrow (n = 12) |
Большинство CHOP и CHOP-подобные режимы Mostly CHOP and CHOP-like programs |
3-ОВ = 63 % 3-OS = 63 % |
|
|
Индолентные В-клеточные лимфомы с перестройкой IRF4 Indolent B-cell lymphoma with IRF4 rearrangement |
|||||||
|
12 |
[18] |
3 |
38 |
Аксиллярные, паховые лимфоузлы, костный мозг Axillary and inguinal lymph nodes, bone marrow |
В дебюте — R-CHOP+поддерживающая терапия R; в рецидиве — R-F First line R-CHOP+supportive therapy R; second line — R-F |
ПР после 1-й и 2-й линий CR after 1st and 2nd lines of CT |
96 мес. после 1-й линии; 24 мес. после 2-й линии 96 month after 1st line of CT; 24 months after 2nd line of CT |
|
62 |
Паховые лимфоузлы Inguinal lymph nodes |
Удаление; Excision |
ПР CR |
12 |
|||
|
66 |
Забрюшинные лимфоузлы Retroperitoneal lymph nodes |
R-CVP+поддерживающая терапия R R-CVP+ supportive therapy R |
ПР CR |
54 |
|||
|
13 |
[36] |
1 |
69 |
Теменная кость Parietal bone |
Без лечения Without therapy |
ПР CR |
12 |
Notes. Me — median, CT — chemotherapy, OS — overall survival, RT — radiation therapy, CR — complete remission, PR — partial response, R — rituximab, R-F — rituximab + fludarabine, R-CVP — rituximab + cyclophosphamide + vincristine + prednisolone, CD — cyclophosphamide + doxorubicin, CHOE+mtx+AraC — cyclophosphamide + doxorubicin + vincristine + etoposide + methotrexate + cytarabine, MTX — methotrexate, AraC — cytarabine, CHOP — cyclophosphamide + vincristine + doxorubicin + prednisolone, COPAD — cyclophosphamide + doxorubicin + vincristine + prednisolone, NHL BFM90 — high-dose chemotherapy.
Цель настоящей работы — представить клиническое наблюдение больного крупноклеточной В-клеточной лимфомой с перестройкой IRF4.
Клиническое наблюдение
В лаборатории кариологии ФГБУ «НМИЦ гематологии» с 2016 по 2020 г. выполнено FISH-исследование на наличие перестройки IRF4 у 19 больных В-клеточными лимфомами (15 больных ФЛ, из них 11 — с I–II стадиями заболевания; 4 больных ДВККЛ, из них 1 — с I стадией заболевания). Возраст больных составил 18–62 года, медиана — 36 лет. У 1 (0,05 %) из 19 больных выявлена перестройка гена IRF4.
Больной Л., 1994 года рождения. В августе 2018 г. отметил увеличение до 1 см лимфатического узла в верхней трети шеи слева. За медицинской помощью не обращался, лимфатический узел медленно увеличивался в размерах. В декабре 2018 г. появилась общая слабость, ночная потливость, снижение работоспособности. В январе 2019 г. отметил трижды повышение температуры тела до 38 °C, без признаков инфекции, температура нормализовалась самостоятельно. При ультразвуковом исследовании (УЗИ) шейных лимфатических узлов в верхней трети шеи слева выявлены два гипоэхогенных близко расположенных друг к другу лимфатических узла с ровными четкими контурами, размерами 23 × 17 мм и 31 × 17 мм. Выполнена биопсия шейных лимфатических узлов. Лимфатические узлы были удалены не полностью в связи с близким расположением к сосудам шеи. Заподозрена диффузная В-крупноклеточная лимфома. Больной был направлен на консультацию в ФГБУ «НМИЦ гематологии», где предъявил жалобы на общую слабость, снижение работоспособности, быструю утомляемость, ночную потливость. При пальпации в области шеи слева отмечено уплотнение мягких тканей в месте зажившего рубца после биопсии. В остальном по органам и системам патологии не выявлено. По данным позитронно-эмиссионной томографии совмещенной с компьютерной томографией (ПЭТ-КТ), отмечалось накопление радиофармпрепарата в мягких тканях шеи слева в области биопсии SUV 3.6, что соответствовало 5 баллам по шкале Deauville (SUV в печени 2,9).
По данным УЗИ шейных лимфатических узлов после биопсии выявлен единичный лимфатический узел размерами 24 × 5 мм. В анализе крови: гемоглобин — 151 г/л, тромбоциты — 158 × 10 9/л, лейкоциты — 3,7 × 10 9/л (нейтрофилы — 31 %, лимфоциты — 57 %, эозинофилы — 4 %, моноциты — 8 %), СОЭ — 2 мм/час. При иммунофенотипическом исследовании лимфоцитов периферической крови отмечено уменьшение содержания Т-лимфоцитов и поликлональных В-лимфоцитов. Активность лактатдегидрогеназы была в норме. При иммунохимическом исследовании моноклональную секрецию не выявили. Концентрация β2-микроглобулина была в норме. При гистологическом исследовании трепанобиоптата костного мозга не обнаружено поражения костного мозга при лимфоме. По реаранжировкам генов тяжелых цепей иммуноглобулинов В-клеточную клональность в пунктате костного мозга не выявили. При пересмотре гистологических препаратов биоптата шейных лимфатических узлов наблюдали субтотальное нарушение гистоархитектоники, обусловленное нечетко очерченными крупными фолликулоподобными структурами с преобладанием среднего размера и крупных лимфоидных клеток с округло-овальными ядрами с морфологией центробластов (рис. 1 А, 1 Б). В одном гистологическом срезе биоптата визуализировали две четко очерченных фолликулоподобных структуры, окруженные широкой зоной реактивного микроокружения предсуществующей ткани лимфатического узла (рис. 1 B).
При иммуногистохимическом исследовании опухолевые клетки экспрессировали CD20 (интенсивная мембранная реакция), BCL6 (ядерная реакция), MUM1 (мономорфная ядерная реакция) (рис. 2 А, 2 Б), BCL2 (умеренная по интенсивности цитоплазматическая реакция в большей части крупных опухолевых клеток, интенсивная — в мелких Т-клетках микроокружения). Опухолевые клетки не экспрессировали CD10 (при позитивном внутреннем контроле в фибробластических волокнах). При реакции с антителами к c-Myc отмечалась гетерогенная ядерная экспрессия до 30 % позитивных опухолевых клеток. При реакции с антителами к CD23 были позитивны отдельные опухолевые клетки (гетерогенная мембранная экспрессия), сеть ФДК визуализировали только в области двух фолликулоподобных структур. Индекс пролиферативной активности Ki-67 составил 70–80 % позитивных опухолевых клеток (рис. 3 А, 3 Б). Т-клетки (CD3+) были расположены разрозненно и в виде небольших скоплений среди В-клеточного опухолевого пролиферата.
FISH-исследование гистологических препаратов биоптата лимфатического узла проводили с использованием ДНК-зондов DUSP22/IRF4 Breakapart Probe (Cytocell, Великобритания), LSI IGH Break Apart Probe, LSI BCL2 Break Apart Probe, LSI BCL6 Break Apart Probe и LSI MYC Break Apart Probe (Abbott, USA). Выявлены перестройки локусов IRF4/6 р25 (рис. 4) и IgH/14q32 (рис. 5), что с высокой долей вероятности свидетельствовало о наличии диагностической t(6;14)(p25;q32). Транслокаций с вовлечением локусов генов BCL2/18q21, BCL6/3q27 и MYC/8q24 не выявлено. Обнаруженные дополнительные сигналы от неперестроенных локусов BCL2/18q21, BCL6/3q27, MYC/8q24 и отсутствие сигнала от теломерного участка локуса 6 р25 (5’ IRF4) свидетельствовали о наличии дополнительных хромосомных нарушений — трисомии хромосом 3, 8, 18 и делеции 6 р25 во втором гомологе хромосомы 6.
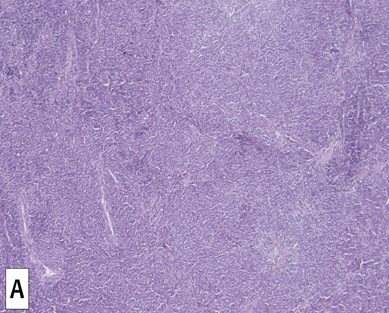
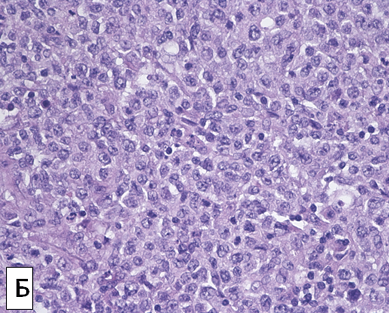
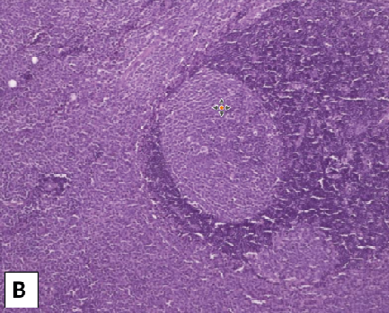
Рисунок 1. Опухолевый субстрат биоптата шейного лимфатического узла: А — нечетко очерченные крупные фолликулоподобные структуры; Б — преобладание среднего размера и крупных лимфоидных клеток с округло-овальными ядрами с морфологией центробластов; В — две четко очерченные фолликулоподобные структуры, окруженные широкой зоной реактивного микроокружения. Окраска гематоксилином и эозином, ×50, ×400, ×100
Figure 1. Tumor substrate in cervical lymph node biopsy: A — vaguely outlined large follicle-like structures; B — predominance of medium size and large lymphoid cells with rounded oval nuclei with centroblasts morpholog; С — two clearly defined follicle-like structures surrounded by a wide zone of reactive microenvironment. Hematoxylin and eosin stain, ×50, ×400, ×100
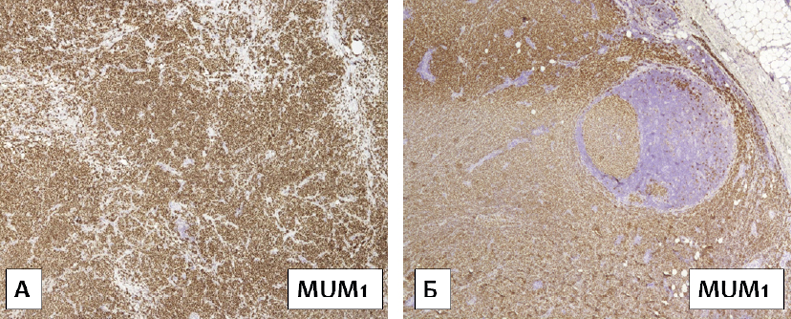
Рисунок 2. Экспрессия опухолевыми клетками MUM1 (мономорфная ядерная реакция) в биоптате шейного лимфатического узла. Иммуноферментный метод, ×200, ×50
Figure 2. Expression of tumor cells MUM1 (monomorphic nuclear reaction) in cervical lymph node biopsy. Immunoenzyme method, ×200, ×50
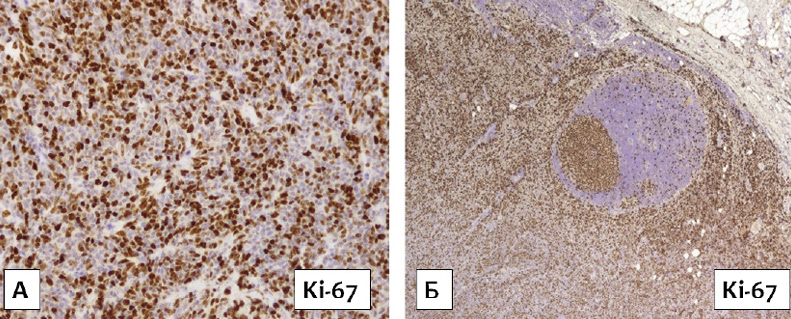
Рисунок 3. Клетки опухолевого субстрата биоптата шейного лимфатического узла с высокой пролиферативной активностью. Реакция с антителом к Ki-67. Иммуноферментный метод, ×200, ×50
Figure 3. Tumor substrate cells in cervical lymph node biopsy with high proliferative activity. Reaction with Ki-67 antibody. Immunoenzyme method, ×200, ×50
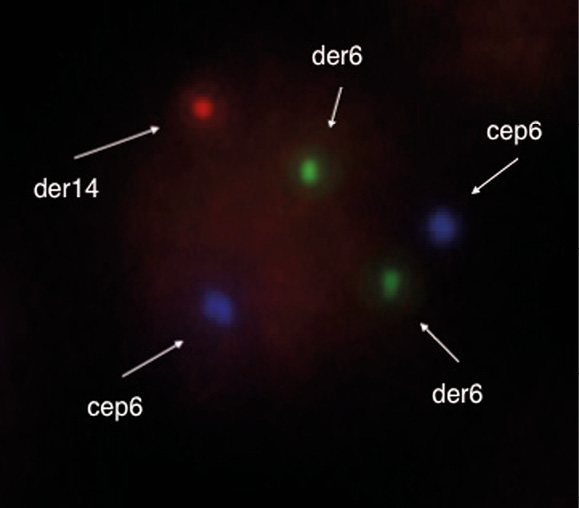
Рисунок 4. Флуоресцентная гибридизация in situ опухолевых клеток биоптата шейного лимфатического узла. Транслокация с вовлечением локуса IRF4/6p25 и делеция р25 второго гомолога хромосомы 6. Два голубых сигнала от центромеры хромосомы 6; один зеленый сигнал от центромерного участка 6p25 на деривате хромосомы 6 и один красный сигнал от теломерного участка 6p25 на деривате хромосомы 14 в результате транслокации; второй зеленый сигнал от центромерного участка 6p25 на деривате хромосомы 6 в результате делеции
Figure 4. Fluorescence hybridization in situ of tumor cells in cervical lymph node biopsy. Translocation involving the IRF4/6p25 locus and deletion of p25 of the second homologue of chromosome 6. Two blue signals from the centromere of chromosome 6; one green signal from the centromere region 6p25 on the derivative of chromosome 6 and one red signal from the telomeric region 6p25 on the derivative of chromosome 14 as a result of translocation; the second green signal from the centromeric region of 6p25 on the derivative of chromosome 6 as a result of a deletion
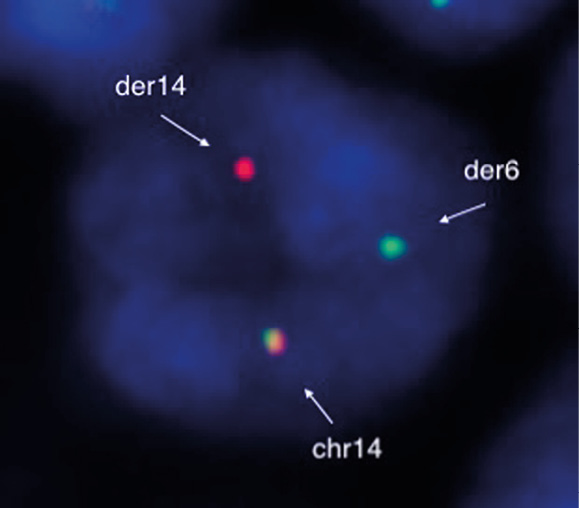
Рисунок 5. Флуоресцентная гибридизация in situ опухолевых клеток биоптата шейного лимфатического узла. Транслокация с вовлечением локуса IgH/14q32. Слитный сигнал от локуса 14q32 на нормальной хромосоме 14; красный сигнал от центромерного участка 14q32 на деривате хромосомы 14; зеленый сигнал от теломерного участка 14q32 на деривате хромосомы 6
Figure 5. Fluorescence hybridization in situ of tumor cells in cervical lymph node biopsy. Translocation involving the IgH/14q32 locus. A fused signal from the 14q32 locus on normal chromosome 14; a red signal from the centromeric region 14q32 on the derivative of chromosome 14; green signal from the telomeric region 14q32 on the derivative of chromosome 6
Таким образом, у больного была диагностирована крупноклеточная В-клеточная лимфома с перестройкой IRF4, с вовлечением шейных лимфатических узлов слева, I Ba стадии. Обращало внимание несоответствие между клиническими и лабораторными характеристиками: морфологическая картина агрессивной лимфомы в биоптате шейного лимфатического узла в сочетании с длительным 6-месячным анамнезом заболевания и небольшими размерами лимфатических узлов, а также наличие В-симптомов при нормальной активности лактатдегидрогеназы и концентрации β2-микроглобулина крови. Учитывая наличие В-симптомов и неполное удаление шейных лимфатических узлов, с марта по май 2019 г. больному проведено 4 курса по программе «R-CHOP-21». После 1-го курса уплотнение в области рубца на шее слева при пальпации не определялось. После 2-го курса регрессировали ночная потливость и общая слабость. По данным ПЭТ-КТ после 4 курсов патологическая метаболическая активность в области лимфатических узлов головы и шеи, а также в других областях не определялась. Констатирован полный метаболический ответ. Поддерживающая терапия ритуксимабом не проводилась. В течение 26 мес. сохраняется ремиссия заболевания.
Обсуждение
Представлено редкое наблюдение IRF4-позитивной лимфомы, клинические, морфологические и генетические особенности которой соответствовали описанию новой нозологической формы, предложенной классификацией ВОЗ [17]. Крупноклеточная В-клеточная лимфома с перестройкой IRF4 — редко встречающаяся патология, однако частота ее встречаемости неизвестна, поскольку исследование на наличие перестройки IRF4 не выполняется у всех больных ДВККЛ и ФЛ 3-го цитологического типа.
Для подтверждения данного варианта лимфомы выполняют цитогенетическое исследование, при котором обнаруживают перестройку локуса гена IRF4. Прогностическое значение данной перестройки при В-клеточных лимфомах противоречиво и нуждается в дальнейших исследованиях. Лимфома с перестройкой IRF4 имеет свой уникальный молекулярно-генетический профиль [1], что отражается на исходах заболевания. Негативное значение экспрессии белка MUM1 при IRF4-позитивной лимфоме нивелируется другими неизвестными механизмами, что подтверждается благоприятным исходом лечения при использовании неинтенсивных режимов химиотерапии. Особенностью данного клинического наблюдения является преимущественно диффузный характер роста опухолевых клеток в биоптате лимфатического узла в сочетании с индолентным течением заболевания, а также наличие цитогенетических аберраций обоих гомологов хромосомы 6: перестройки IRF4 и делеции 6p25.
Тактика лечения IRF4-позитивной лимфомы в настоящее время не разработана. Применение неинтенсивных курсов химиотерапии в сочетании или без лучевой терапии приводит к достижению длительных ремиссий [21]. У детей описаны единичные наблюдения с благоприятным исходом при вовлечении небных миндалин после тонзиллэктомии без химиотерапии [17]. Учитывая наличие у описанного больного В-симптомов и неполное удаление шейных лимфатических узлов, проведена химиотерапия по программе «R-CHOP-21» позволившая достичь полную ремиссию заболевания, которая сохраняется в течение 26 мес.
Список литературы
1. Pittaluga S., Harris N., Siebert R., et al. Large B-cell lymphoma with IRF4 rearrangement. In: Swerdlow S.H., Campo E.H.N. (Eds). WHO Classifi cation of tumours of haematopoietic and lymphoid tissues. Lyon, France: International Agency for Research on Cancer; 2017: 280–1.
2. Tanaka N., Taniguchi T. The interferon regulatory factors and oncogenesis. Semin Cancer Biol. 2000; 10(2): 73–81. DOI: 10.1006/scbi.2000.0310.
3. Grossman A., Mittrücker H.W., Nicholl J., et al. Cloning of human lymphocyte-specifi c interferon regulatory factor (hLSIRF/hIRF4) and mapping of the gene to 6p23-p25. Genomics. 1996; 37(2): 229–33. DOI: 10.1006/geno.1996.0547.
4. Iida S., Rao P.H., Butler M., et al. Deregulation of MUM1/IRF4 by chromosomal translocation in multiple myeloma. Nat Genet. 1997; 17(2): 226–30. DOI: 10.1038/ng1097-226.
5. Yoshida S., Nakazawa N., Iida S., et al. Detection of MUM1/IRF4-IgH fusion in multiple myeloma. Leukemia. 1999; 13(11): 1812–6. DOI: 10.1038/sj.leu.2401563.
6. Mittrücker H.W., Matsuyama T., Grossman A., et al. Requirement for the transcription factor LSIRF/IRF4 for mature B and T lymphocyte function. J Immunol. 2017; 199(11): 3717–20. DOI: 10.1126/science.275.5299.540.
7. Saito T., Yamagata T., Takahashi T., et al. ICSAT overexpression is not suffi cient to cause adult T-cell leukemia or multiple myeloma. Biochem Biophys Res Commun. 1999; 260(2): 329–31. DOI: 10.1006/bbrc.1999.0911.
8. Grumont R.J., Gerondakis S. Rel induces interferon regulatory factor 4 (IRF-4) expression in lymphocytes: Modulation of interferon-regulated gene expression by Rel/nuclear factor B. J Exp Med. 2000; 191(8): 1281–91. DOI: 10.1084/jem.191.8.1281.
9. Shaffer A.L., Wright G., Yang L., et al. A library of gene expression signatures to illuminate normal and pathological lymphoid biology. Immunol Rev. 2006; 210(1): 67–85. DOI: 10.1111/j.0105-2896.2006.00373.x.
10. Falini B., Fizzotti M., Pucciarini A., et al. A monoclonal antibody (MUM1p) detects expression of the MUM1/IRF4 protein in a subset of germinal center B cells, plasma cells, and activated T cells. Blood. 2000; 95(6): 2084–92.
11. Martinez A., Pittaluga S., Rudelius M., et al. Expression of the interferon regulatory factor 8/ICSBP-1 in human reactive lymphoid tissues and B-cell lymphomas: A novel germinal center marker. Am J Surg Pathol. 2008; 32(8): 1190–200. DOI: 10.1097/PAS.0b013e318166f46a.
12. Gualco G., Weiss L., Bacchi C. MUM1/IRF4: A review. Appl Immunohistochem Mol Morphol AIMM. 2010; 18(4): 301–10. DOI: 10.1097/PAI.0B013E3181CF1126.
13. Satou A., Asano N., Kato S., et al. Prognostic impact of MUM1/IRF4 expression in Burkitt Lymphoma (BL): A reappraisal of 88 BL patients in Japan. Am J Surg Pathol. 2017; 41(3): 389–95. DOI: 10.1097/PAS.0000000000000804.
14. Valsami S., Pappa V., Rontogianni D., et al. A clinicopathological study of Bcell differentiation markers and transcription factors in classical Hodgkin’s lymphoma: A potential prognostic role of MUM1/IRF4. Haematologica. 2007; 92(10):1343–50. DOI: 10.3324/haematol.11523.
15. Xerri L., Bachy E., Fabiani B., et al. Identifi cation of MUM1 as a prognostic immunohistochemical marker in follicular lymphoma using computerized image analysis. Hum Pathol. 2014; 45(10): 2085–93. DOI: 10.1016/j.humpath.2014.06.019.
16. Kridel R., Mottok A., Farinha P., et al. Cell-of-origin of transformed follicular lymphoma. Blood. 2015; 126(18): 2118–27. DOI: 10.1182/blood-2015-06-649905.
17. Salaverria I., Philipp C., Oschlies I., et al. Translocations activating IRF4 identify a subtype of germinal center-derived B-cell lymphoma affecting predominantly children and young adults. Blood. 2011; 118(1): 139–47. DOI: 10.1182/blood-2011-01-330795.
18. Takeuchi K., Sakata S., Asaka R., et al. A low-grade B-cell lymphoma with prolymphocytic/paraimmunoblastic proliferation and IRF4 rearrangement. Haematologica. 2013; 98(3): e32–5. DOI: 10.3324/haematol.2012.076851.
19. Tamura A., Miura I., Iida S., et al. Interphase detection of immunoglobulin heavy chain gene translocations with specifi c oncogene loci in 173 patients with B-cell lymphoma. Cancer Genet Cytogenet. 2001; 129(1): 1–9. DOI: 10.1016/s0165-4608(01)00436-8.
20. Hunt K.E., Hall B., Reichard K.K. Translocations involving MUM1 are rare in diffuse large B-cell lymphoma. Appl Immunohistochem Mol Morphol. 2010;18(2): 109–12. DOI: 10.1097/PAI.0b013e31817fa43c.
21. Ramis-Zaldivar J.E., Gonzalez-Farré B., Balagué O., et al. Distinct molecular profile of IRF4-rearranged large B-cell lymphoma. Blood. 2020; 135(4): 274–86. DOI: 10.1182/blood.2019002699.
22. Salaverria I., Martin-Guerrero I., Burkhardt B., et al. High resolution copy number analysis of IRF4 translocation-positive diffuse large B-cell and follicular lymphomas. Genes Chromosom Cancer. 2013; 52(2): 150–5. DOI: 10.1002/gcc.22014.
23. Level L. De, Bonnet C., Copie-Bergman C., et al. Diffuse large B-cell lymphoma of Waldeyer’s ring has distinct clinicopathologic features: A GELA study. Ann Oncol. 2012; 23(12): 3143–51. DOI: 10.1093/annonc/mds150.
24. Liu Q., Salaverria I., Pittaluga S., et al. Follicular lymphomas in children and young adults: A comparison of the pediatric variant with usual follicular lymphoma. Am J Surg Pathol. 2013; 37(3): 333–43. DOI: 10.1038/jid.2014.371.
25. Carbone P.P., Kaplan H.S., Musshoff K., et al. Report of the Committee on Hodgkin’s disease staging classifi cation. Cancer Res. 1971; 31(11): 1860–1.
26. Chisholm K.M., Termuhlen A., Perkins S.L., et al. IRF4 translocation status in pediatric follicular and diffuse large B-cell lymphoma patients enrolled in Children’s Oncology Group trials. Pediatr Blood Cancer. 2019; 66(8): e27770. DOI: 10.1002/pbc.27770.
27. Verma A., Epari S., Gujral S., et al. An unusual presentation of large B-cell lymphoma with interferon regulatory factor 4 gene rearrangement. Indian J Pathol Microbiol. 2018; 61(2): 271–4. DOI: 10.4103/IJPM.IJPM_194_17.
28. Hans C.P., Weisenburger D.D., Greiner T.C., et al. Confi rmation of the molecular classifi cation of diffuse large B-cell lymphoma by immunohistochemistry using a tissue microarray. Blood. 2004; 103(1): 275–82. DOI: 10.1182/blood-2003-05-1545.
29. NCCN Clinical Practice Guidelines in Oncology. B-cell lymphomas. Version 2.2020. https://www.nccn.org/professionals/physician_gls/pdf/b-cell.pdf.
30. Quintanilla-Martinez L., Sander B., Chan J.K.C., et al. Indolent lymphomas in the pediatric population: Follicular lymphoma, IRF4/MUM1+ lymphoma, nodal marginal zone lymphoma and chronic lymphocytic leukemia. Virchows Arch. 2016; 468(2): 141–57. DOI: 10.1007/s00428-015-1855-z.
31. Man J., Wang Y., Zhai X., et al. Large B-cell lymphoma with IRF4 rearrangement: A special tonsillar lymphoma in children. Pediatr Hematol Oncol J. 2019; 4(4): 77–81. DOI: 10.1016/j.phoj.2019.12.001.
32. Chonabayashi K., Tamori S., Taniwaki M., et al. Refractory IGκ/IRF4-positive DLBCL with CDKN2A/2B deletion. Ann Hematol. 2014; 93(5): 893–4. DOI: 10.1007/s00277-013-1889-8.
33. Vincent G., Richebourg S., Cloutier S., et al. Large B-cell lymphoma with IRF4 rearrangement: From theory to practice. AJSP Rev Reports. 2019; 24(5): 240. DOI: 10.1097/PCR.0000000000000329.
34. Yu Y.T., Sakata S., Takeuchi K., et al. Tonsillar follicular large B-cell lymphoma with IRF4 rearrangement causing sleep apnoea. J Clin Pathol. 2020; 73(2): 120–1. DOI: 10.1136/jclinpath-2019-205915.
35. Ma Z., Shi Y., Pang X., et al. Clinicopathologic features and prognostic analysis of Waldeyer ring B-cell lymphoma. Medicine (Baltomore). 2020; 99(2): e18670. DOI: 10.1097/MD.0000000000018670.
36. Nasim M.M., Chalif D.J., Demopoulos A.M., et al. Primary low-grade B-cell lymphoma of skull with translocation between immunoglobulin and interferon regulatory factor 4 genes. Int J Surg Pathol. 2020; 28(3): 330–5. DOI: 10.1177/1066896919883013.
Об авторах
Л. В. ПластининаРоссия
Пластинина Любовь Васильевна*, кандидат медицинских наук, гематолог консультативного гематологического отделения с дневным стационаром по проведению интенсивной высокодозной химиотерапии
125167, Москва
Т. Н. Моисеева
Россия
Моисеева Татьяна Николаевна, кандидат медицинских наук, гематолог, заведующая консультативным гематологическим отделением с дневным стационаром по проведению интенсивной высокодозной химиотерапии
125167, Москва
Л. С. Аль-Ради
Россия
Аль-Ради Любовь Саттаровна, кандидат медицинских наук, врач-гематолог консультативного гематологического отделения с дневным стационаром по проведению интенсивной высокодозной химиотерапии
125167, Москва
А. М. Ковригина
Россия
Ковригина Алла Михайловна, доктор биологических наук, заведующая патологоанатомическим отделением
125167, Москва
Т. Н. Обухова
Россия
Обухова Татьяна Никифоровна, кандидат медицинских наук, заведующая лабораторией кариологии
125167, Москва
С. Р. Горячева
Россия
Горячева Светлана Рудольфовна, кандидат медицинских наук, гематолог консультативного гематологического отделения с дневным стационаром по проведению интенсивной высокодозной химиотерапии
125167, Москва
И. А. Шуплецова
Россия
Шуплецова Ирина Александровна, кандидат медицинских наук, врач патологоанатомического отделения
125167, Москва
А. У. Магомедова
Россия
Магомедова Аминат Умарасхабовна, доктор медицинских наук, ведущий научный сотрудник отделения интенсивной высокодозной химиотерапии гемобластозов
125167, Москва
С. К. Кравченко
Россия
Кравченко Сергей Кириллович, кандидат медицинских наук, заведующий отделением интенсивной высокодозной химиотерапии гемобластозов
125167, Москва
Рецензия
Для цитирования:
Пластинина Л.В., Моисеева Т.Н., Аль-Ради Л.С., Ковригина А.М., Обухова Т.Н., Горячева С.Р., Шуплецова И.А., Магомедова А.У., Кравченко С.К. Крупноклеточная В-клеточная лимфома с перестройкой IRF4. Гематология и трансфузиология. 2021;66(3):445-457. https://doi.org/10.35754/0234-5730-2021-66-3-445-457
For citation:
Plastinina L.V., Moiseeva T.N., Al-Radi L.S., Kovrigina A.M., Obukhova T.N., Goryacheva S.R., Shupletsova I.A., Magomedova A.U., Kravchenko S.K. Large B-cell lymphoma with IRF4 rearrangement. Russian journal of hematology and transfusiology. 2021;66(3):445-457. (In Russ.) https://doi.org/10.35754/0234-5730-2021-66-3-445-457











































