ОРИГИНАЛЬНЫЕ СТАТЬИ
Введение. Современная терапия рецидивов и резистентных форм острых Т-клеточных лимфобластных лейкозов/ лимфом (Т-ОЛЛ/ЛБЛ) является малоэффективной. Использование неларабина позволяет улучшить результаты терапии у больных с рефрактерным течением/рецидивом Т-ОЛЛ/ЛБЛ.
Цель исследования — оценить эффективность и токсичность терапии неларабином в сочетании с этопозидом и циклофосфамидом у взрослых больных с рефрактерным течением/рецидивом Т-ОЛЛ/ЛБЛ.
Материалы и методы. С 2012 по 2018 гг. 10 больным в возрасте от 19 лет до 41 года с рефрактерным течением/ рецидивом Т-ОЛЛ проводили терапию неларабином. Выполнены от 1 до 3 курсов химиотерапии, включавших неларабин 650 мг/м2 (с 1-го по 5-й день), этопозид 100 мг/м2 и циклофосфамид 440 мг/м2 (с 8-го по 12-й день). Всем больным, достигшим полной ремиссии (ПР), была проведена трансплантация аллогенных гемопоэтических стволовых клеток (алло-ТГСК). Оценку токсических осложнений (миелосупрессия, нейротоксичность, частота развития инфекционных осложнений) проводили после каждого курса химиотерапии.
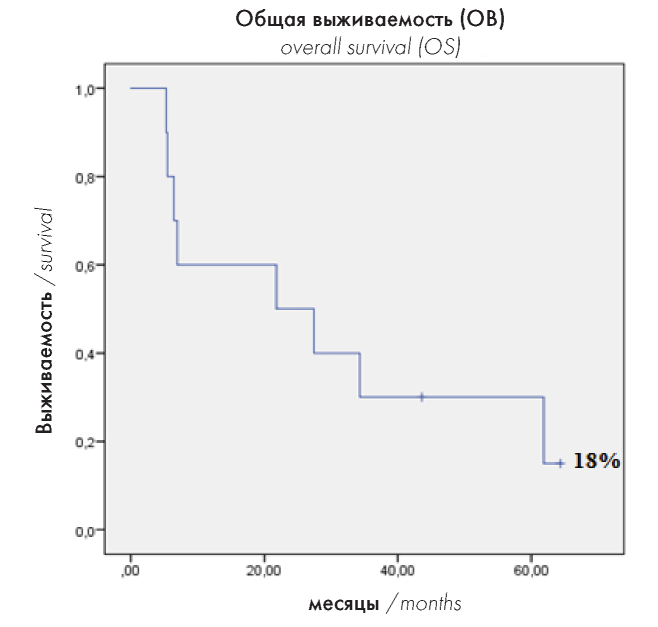
Результаты. ПР после 1–2 курсов химиотерапии была достигнута у 6 (60 %) из 10 больных. Всем 6 больным, достигшим ПР, была выполнена алло-ТГСК. У 3 (50 %) из 6 больных после алло-ТГСК диагностирован ранний рецидив заболевания, 1 из 6 больных умер от инфекционных осложнений при сохраняющейся ПР заболевания. Только 2 больных находятся под наблюдением в течение полутора лет после алло-ТГСК. Общая выживаемость (ОВ) составила 18 % в течение 5 лет от момента диагностики рецидива заболевания. Среди токсических осложнений у всех больных отмечали миелосупрессию и инфекционные осложнения. Нейротоксичность зарегистрирована у 3 (30 %) из 10 больных, причем у 2 из них ее отмечали после каждого курса, а у 1 — только после 3-го курса с неларабином.
Заключение. Применение неларабина для лечения резистентных форм/рецидивов Т-ОЛЛ/ЛБЛ позволяет достичь ПР заболевания в 60 % случаев и выполнить алло-ТГСК. Однако долгосрочные результаты не столь оптимистичны.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Финансирование: исследование не имело спонсорской поддержки.
Введение. Проведение трансплантации аллогенных гемопоэтических стволовых клеток (алло-ТГСК) невозможно без центрального венозного катетера (ЦВК).
Цель — определить тактику обеспечения венозного доступа при проведении алло-ТГСК.
Материалы и методы. В проспективное нерандомизированное одноцентровое исследование включены 146 больных (70 мужчин и 76 женщин, медиана возраста 37 лет), которым выполнена первая алло-ТГСК. Перед кондиционированием устанавливали один из видов ЦВК: силиконовые двухпросветные туннелируемые катетеры Хикмана или Леонарда (Bard Access System) или полиуретановые нетуннелируемые ЦВК (Certofix Duo или катетеры с антибактериальным покрытием Certofix “Protect” Duo, В. Вraun). Регистрировали ранние осложнения, механические осложнения, катетер-ассоциированные тромбозы (КАТ), катетер-ассоциированную инфекцию (КАИК), туннельную инфекцию и инфекцию выходного отверстия.
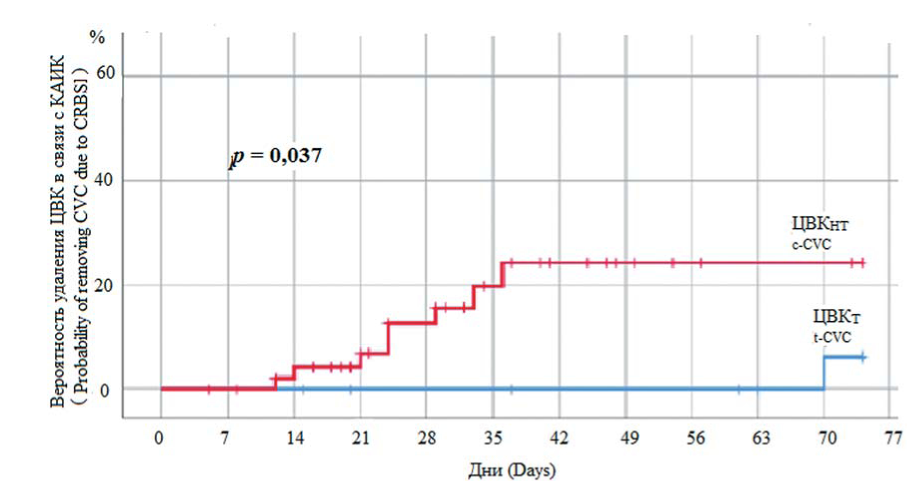
Результаты. Всего установили 320 ЦВК (146 перед алло-ТГСК и 174 — в посттрансплантационном периоде), из них 259 нетуннелируемых и 61 туннелируемый ЦВК. Нетуннелируемые ЦВК эксплуатировали от 1 до 123 дней (медиана 22 дня), туннелируемые ЦВК — 9–621 день (медиана 146 дней). При использовании нетуннелируемых ЦВК выявлено 2,7 % (1,0/1000 катетеро-дней) механических осложнений и 9 % КАТ (1,4/1000 катетеро-дней). При использовании туннелируемых ЦВК были следующие осложнения: случайное удаление — 1 (1,6 %), разрыв катетера — 4 (6,5 %), КАТ вывили у 5 (8,2 %) больных (0,3/1000 катетеро-дней); обструкция катетера — у 18 (29,5 %) больных, из них у 14 (77,7 %) функция ЦВК восстановлена, у 4 (22,3 %) — катетер удален. Инцидентность КАИК нетуннелируемых ЦВК — 4,4/1000 катетеро-дней, туннелируемых ЦВК — 1,5/1000 катетеро-дней. Не выявлено значимых различий вероятности развития КАИК между нетуннелируемыми ЦВК с антибактериальным покрытием и без покрытия (р = 0,298), а также между нетуннелируемыми и туннелируемыми ЦВК в первые 28 дней от момента установки (р = 0,424). Риск развития КАИК при использовании туннелируемых ЦВК увеличивался после 150-го дня эксплуатации.
Заключение. Проведение алло-ТГСК возможно с использованием любого типа ЦВК. Не выявлено преимуществ использования нетуннелируемых ЦВК с антибактериальным покрытием по сравнению с нетуннелируемыми ЦВК без антибактериального покрытия. Применение туннелируемых ЦВК позволяет, в отличие от нетуннелируемых ЦВК, использовать один катетер на протяжении всего трансплантационного и посттрансплантационного периодов, при этом длительность использования туннелируемого ЦВК не должна превышать 150 дней, потому что при более длительном использовании резко увеличивается риск его инфицирования.
Финансирование: исследование не имело спонсорской поддержки.
Введение. Трансплантация гемопоэтических стволовых клеток является терапией выбора многих больных злокачественными заболеваниями системы крови. Одним из наиболее тяжелых осложнений у них является острая реакция «трансплантат против хозяина» (РТПХ) с поражением кишечника. Однако принятый в настоящее время в качестве диагностического критерия объем стула за сутки не всегда позволяет вовремя установить диагноз.
Цель — исследовать возможность применения ультразвукового исследования кишечника для диагностики острой РТПХ с поражением кишечника.
Материалы и методы. В исследование было включено 50 больных, перенесших трансплантацию аллогенных гемопоэтических стволовых клеток. У 40 имелись клинические признаки РТПХ с поражением кишечника (диарея >500 мл/сут). Контрольная группа включала 10 больных после трансплантации аллогенных гемопоэтических стволовых клеток, у которых отсутствовали признаки поражения желудочно-кишечного тракта. Всем больным проводили ультразвуковое измерение толщины стенки кишечника.
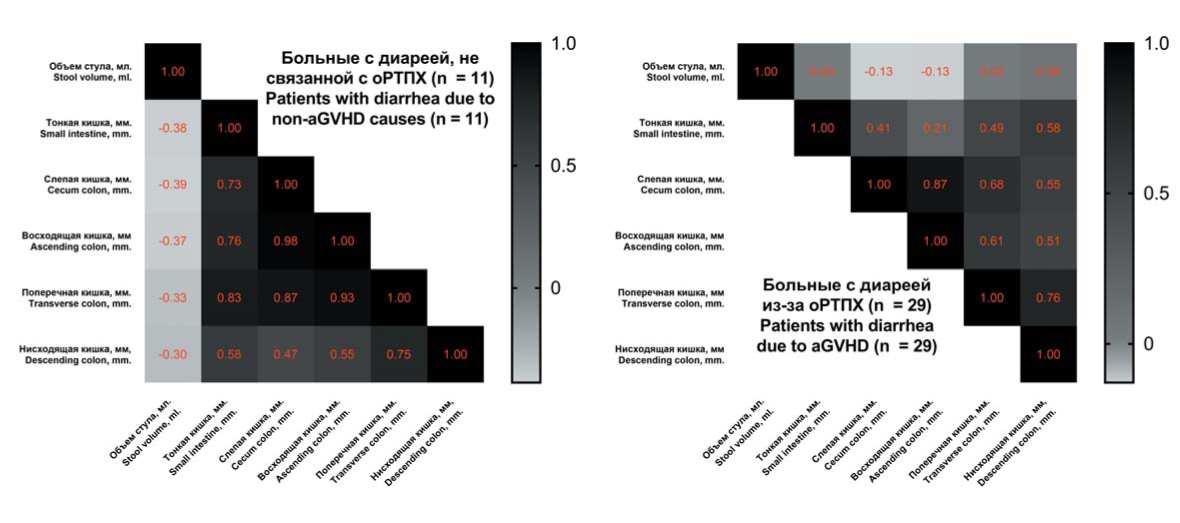
Результаты. Было сформировано 3 группы больных: больные с острой РТПХ, диареей вирусного или инфекционного генеза, диареей вследствие токсического воздействия химиопрепаратов. По результатам исследования у больных с острой РТПХ стенки всех отделов кишечника были значимо толще, по сравнению с контрольной группой и с больными с диареей вследствие других причин.
Заключение. Утолщение стенки слепой кишки более 3,25 мм, выявленное ультразвуковым методом, может использоваться в качестве диагностического признака РТПХ с поражением кишечника.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Финансирование: исследование не имело спонсорской поддержки.
Введение. У больных хроническим миелолейкозом (ХМЛ) изменены свойства клеток-предшественниц стромального микроокружения — мультипотентные мезенхимальные стромальные клетки (ММСК) и колониеобразующие единицы фибробластов (КОЕф).
Цель — сравнительное изучение клеток-предшественниц стромального микроокружения ММСК и КОЕф, полученных из костного мозга больных ХМЛ в дебюте заболевания, через год после начала лечения и на длительных сроках лечения ингибиторами тирозиновых киназ (ИТК).
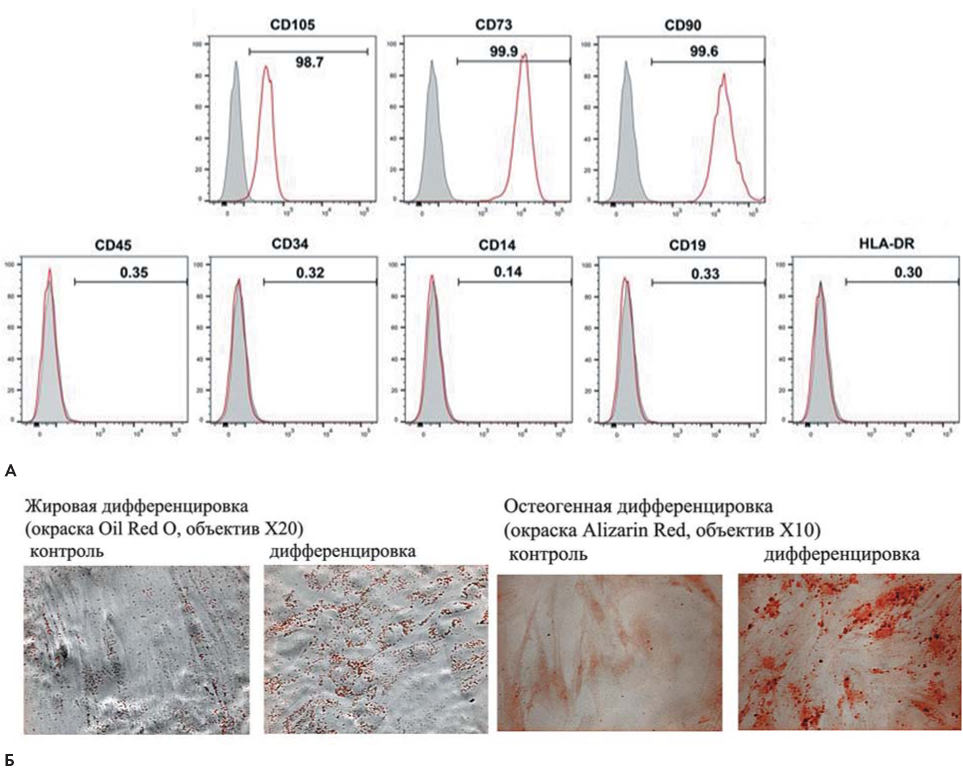
Материалы и методы. Были проанализированы характеристики ММСК и концентрация КОЕф в костном мозге больных ХМЛ, а также относительный уровень экспрессии генов (REL), связанных с дифференцировкой и участвующих в регуляции кроветворения. Анализ проводили в дебюте заболевания, через год после начала лечения, через 3–8 лет и через 9–16 лет терапии ИТК. В качестве контроля использовали ММСК и КОЕф здоровых доноров.
Результаты. Концентрация КОЕф в дебюте заболевания не отличалась от таковой у доноров, однако в колониях из КОЕф был увеличен относительный уровень экспрессии генов, относящихся к дифференцировке. Через год после начала лечения ИТК концентрация КОЕф снижалась в 4 раза, а затем увеличивалась и достигала нормальных значений через 8 лет приема ИТК. Суммарная клеточная продукция ММСК не была изменена в дебюте заболевания, но снижалась через год приема ИТК с последующим восстановлением. В ММСК больных была изменена экспрессия многих генов: экспрессия REL LIF была увеличена в 10, а JAG1 — в 2 раза, экспрессия REL LIF снижалась по мере лечения, но всегда оставалась выше, чем в ММСК доноров, а экспрессия JAG1 нормализовывалась. В ММСК больных, достигших глубокого молекулярного ответа (ГМО) в течение 17 месяцев лечения, экспрессия REL LIF в дебюте заболевания была в три раза ниже, чем у тех, кто не достиг ГМО за 50 месяцев, а JAG1 не отличался от доноров.
Заключение. Изменения в стромальных клетках предшественницах связаны не только с влиянием опухолевых клеток, но и с лечением ИТК. Нормальный уровень экспрессии JAG1 и сниженный уровень экспрессии LIF в ММСК больных ХМЛ в дебюте заболевания могут быть предикторами достижения ГМО.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Финансирование: исследование не имело спонсорской поддержки.
Введение. Первичная иммунная тромбоцитопения (идиопатическая тромбоцитопеническая пурпура — ИТП) — редкое аутоиммунное заболевание, основным клиническим проявлением которого является геморрагический синдром различной степени тяжести. Терапия ИТП направлена на купирование геморрагических проявлений и сохранение качества жизни больного. В Российской Федерации (РФ) данные о заболеваемости, особенностях клинического течения и ответе на терапию больных ИТП отсутствуют.
Цель — оценка эпидемиологических и клинических характеристик ИТП у взрослого населения РФ.
Материалы и методы. Клинические и лабораторные данные электронной индивидуальной карты больного ИТП, включенного в многоцентровое проспективное наблюдательное когортное исследование «Эпидемиологические и клинические характеристики ИТП у взрослых в России» с 2014 по 2017 гг. Обработка данных проводилась с использованием методов описательной статистики, частотного, дисперсионного и событийного анализа. Расчеты проводились с помощью процедур статистического пакета SAS V9.4.
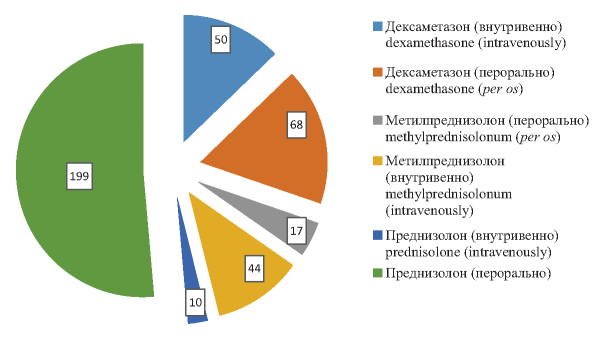
Результаты. Заболеваемость ИТП в трех выбранных регионах РФ среди взрослого населения в среднем составила 2,09 на 100 тыс. человек в год. Наибольшая заболеваемость в половозрастных группах была отмечена у женщин моложе 40 лет и составила 2,7 на 100 тыс. У мужчин отмечено постепенное увеличение заболеваемости с 1,09 до 2,5 на 100 тыс. в группе старше 60 лет. Обнаружена достоверная взаимосвязь между риском развития, тяжестью геморрагического синдрома и количеством тромбоцитов крови в дебюте заболевания (p < 0,0001). В 92,2 % случаев в качестве первой линии терапии назначались глюкокортикостероидные гормоны. Анализ методов, используемых в качестве второй линии терапии, показал, что хотя спленэктомия выполняется относительно часто, вероятность ее выполнения в течение последних трех лет снизилась с 26 до 17 %, при этом доля больных, получающих агонисты тромбопоэтиновых рецепторов, увеличилась с 5,9 до 45,7 %.
Заключение: заболеваемость ИТП в трех выбранных регионах РФ сопоставима с таковой в других странах Европы.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
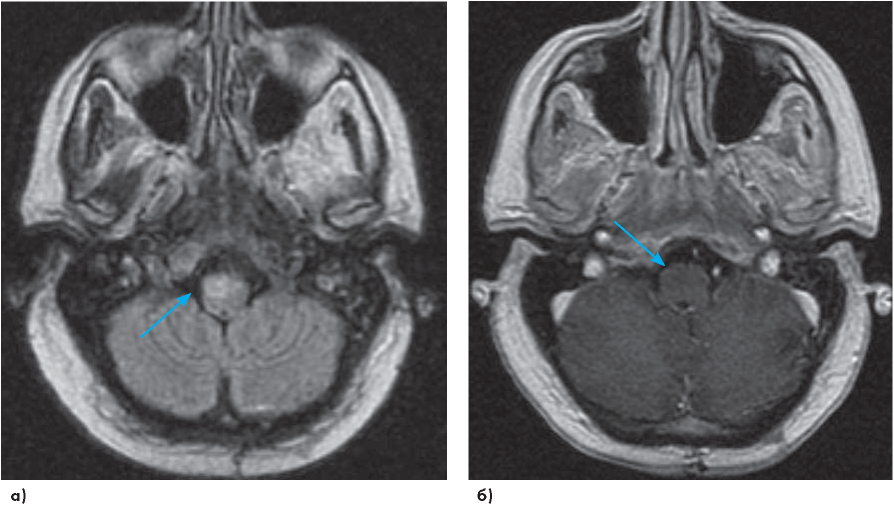
Введение. Основой индукционной химиотерапии (ХТ) первичной диффузной В-крупноклеточной лимфомы центральной нервной системы (ПДВККЛ ЦНС) является применение метотрексата в высоких дозах. Оптимальной стратегией консолидации является высокодозная ХТ с последующей трансплантацией аутологичных гемопоэтических стволовых клеток (ауто-ТГСК). Наиболее эффективным режимом кондиционирования являются комбинации химиопрепаратов с включением тиотепы.
Цель: предоставить собственный опыт применения ауто-ТГСК/TBC у больных ПДВККЛ ЦНС.
Методы. С 2015 по 2019 г. в проспективное исследование CNS-2015 было включено 20 больных в возрасте от 20 до 52 лет (медиана 42 года). Соотношение мужчины/женщины = 13/7. Соматический статус у 17 (85 %) больных соответствовал 0–1 баллу по шкале ECOG и только у 3 (15 %) — 4 баллам. Согласно критериям прогностической системы MSKCC, 18 (90 %) больных были отнесены к группе низкого риска и 2 (10 %) больных — к группе среднего риска.
Результаты. Всем больным, включенным в исследование, было проведено 3–5 циклов ХТ с метотрексатом в высоких дозах, винкристином, прокарбазином и ритуксимабом (R-MPV) и выполнена ауто-ТГСК с режимом кондиционирования TBC (тиотепа, бусульфан, циклофосфамид). Перед началом ауто-ТГСК у 15 их 20 больных, у которых полностью завершили индукционную ХТ, была достигнута полная ремиссия, а у 5 — частичная ремиссия. У 5 больных с исходным частичным ответом после ауто-ТГСК удалось достичь полной ремиссии. Всем больным проводилась поддерживающая терапия темозоломидом в течение 2 лет. При медиане наблюдения 17 (1–46) месяцев 18 больных живы и находятся в ремиссии заболевания. Двое больных, у которых развился рецидив заболевания (+4 и +5 месяцы после ауто-ТГСК) и не было ответа на вторую линию ХТ и лучевую терапию, умерли через 24 и 26 месяцев после ауто-ТГСК.
Заключение. Режим R-MPV является эффективным методом лечения больных ПДВККЛ ЦНС, не сопровождающийся тяжелой токсичностью. Применение высокодозной ХТ по программе TBC позволяет достичь высокой частоты ремиссий, при этом смертность, связанная с лечением, в группе больных, включенных в протокол, была равна 0 %.
Введение. Одним из основных факторов патогенеза ожоговой болезни являются нарушения микроциркуляции и гемостаза, причиной которых служит повышение агрегации тромбоцитов. Механизмы усиления агрегации тромбоцитов малоизучены. Основные результаты получены у взрослых больных в раннем периоде ожоговой болезни, поскольку у больных детского возраста аналогичные данные отсутствуют. Имеются данные о связи размеров тромбоцитов (MPV) с их функциональными возможностями.
Цель — исследование спонтанной и АДФ-индуцированной агрегации тромбоцитов в зависимости от их размеров при ожоговой болезни у детей.
Материалы и методы. У детей в возрасте от 3 до 17 лет с площадью ожога от 10 до 70 % поверхности тела изучали агрегацию и размеры тромбоцитов в раннем периоде и до выписки. Спонтанную агрегацию тромбоцитов исследовали в условиях искусственного сдвигового потока, а АДФ-индуцированную агрегацию — турбидиметрическим методом. Изучение размеров тромбоцитов проводили кондуктометрическим методом.
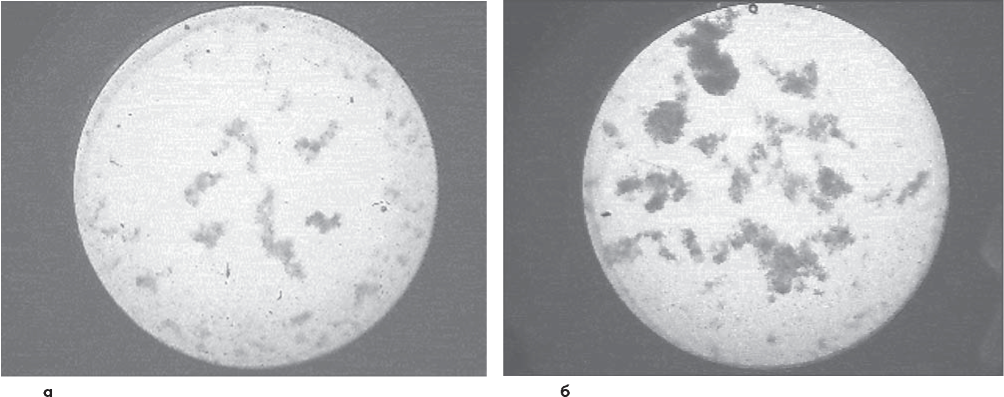
Результаты. У детей при ожоговой болезни спонтанная агрегация тромбоцитов значительно возрастает. Впервые оценили интегральную оптическую плотность образовывающихся агрегатов, их площадь и периметр. Эти показатели оставались повышенными даже при полном закрытии ожоговых ран. Изменения АДФ-индуцированной агрегации тромбоцитов носили при ожоговой болезни разнонаправленный характер. Средний объем тромбоцитов (MPV) возрастал в остром периоде ожоговой болезни, снижался в периоде токсемии и нормализовался к моменту выписки больных. Изменения MPV не отражались на динамике агрегационных свойств тромбоцитов. Отсутствовала зависимость степени агрегации от выраженности гиперфибриногенемии. В крови ожоговых больных имелось большое количество активированных тромбоцитов, что являлось причиной усиления их спонтанной агрегации, не требовавшей участия экзогенных индукторов.
Заключение. У детей после термической травмы наблюдалось усиление спонтанной агрегации тромбоцитов, сохранявшееся до полного закрытия ожоговых ран. Причиной усиления спонтанной агрегации тромбоцитов являлось значительное увеличение количества активированных тромбоцитов.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Финансирование: исследование не имело спонсорской поддержки.
ОБЗОРЫ ЛИТЕРАТУРЫ
Ведение. Значение открытия металлопротеазы ADAMTS-13 выходит за рамки представления о ее ключевой роли в патогенезе тромботической тромбоцитопенической пурпуры (ТТП), имеются данные о наличии связи между снижением активности ADAMTS-13 и тромботическими событиями при остром инфаркте миокарда и ишемическом инсульте.
Цель обзора — обобщение современной информации о структуре и функции металлопротеазы ADAMTS-13.
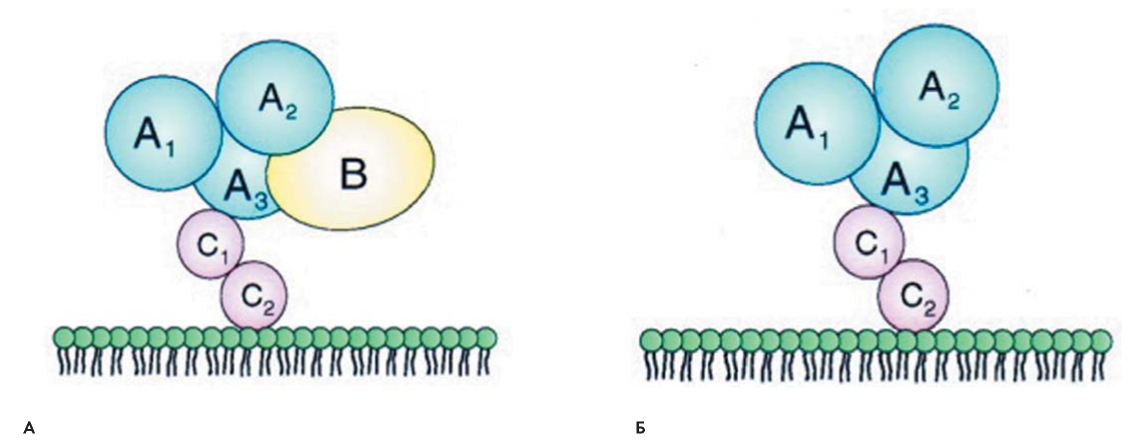
Основные сведения. Биологической функцией протеазы ADAMTS-13 является расщепление сверхкрупных мультимеров фактора Виллебранда. Основой для понимания функции расщепляющей фактор Виллебранда протеазы явилась демонстрация того, что дефицит ее является причиной развития ТТП. ADAMTS-13 имеет доменную структуру. Установлено функциональное значение большинства доменов ADAMTS-13, ключевая роль взаимодействия ADAMTS-13 и WF в регуляции гемостаза. Конформационная активация протеазы ADAMTS-13 фактором Виллебранда является важным аспектом реализации ее функции. После попадания в кровоток сверхкрупные мультимеры фактора Виллебранда быстро принимают закрытую конформацию, которая становится очень устойчивой к протеолизу ADAMTS-13 при отсутствии напряжения сдвига. Плазменные сверхкрупные мультимеры фактора Виллебранда восстанавливает свою чувствительность к ADAMTS-13 при воздействии высокого напряжения сдвига жидкости, которое разворачивает центральный домен А2 фактора Виллебранда. Развертывание молекулы фактора Виллебранда под воздействием напряжения сдвига открывают в домене А2 ранее скрытые экзосайты, которые постепенно увеличивают сродство связывания между ADAMTS-13 и фактором Виллебранда. Механизм выработки аутоантител против ADAMTS-13 неизвестен и требует дальнейшего изучения. Маскировка криптических эпитопов в замкнутой конформации ADAMTS-13 предотвращает образование аутоантител. Раннее антигенное распознавание ADAMTS-13 происходит через поверхностные обнаженные эпитопы в С-концевых доменах. Более подробная информация о механизмах взаимодействия между ADAMTS-13 и фактором Виллебранда может улучшить понимание механизмов регуляции свертывающей системы.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Финансирование: исследование не имело спонсорской поддержки.
КЛИНИЧЕСКИЕ НАБЛЮДЕНИЯ
Введение. Варфарин-индуцированный некроз кожи является редким осложнением лечения варфарином.
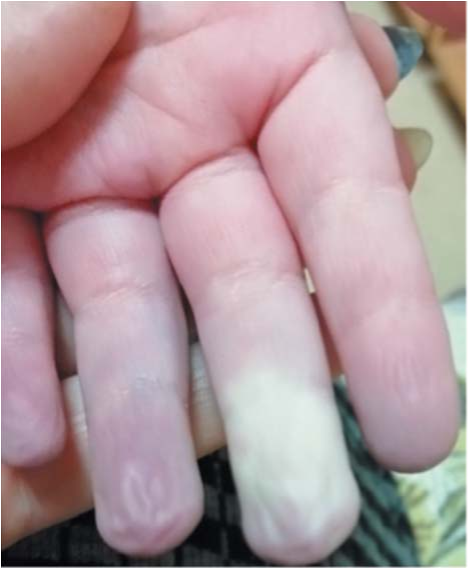
Цель — представить клиническое наблюдение возникновения и успешного лечения атипичного варфарининдуцированного некроза кожи у ребенка с врожденным пороком сердца.
Основные сведения. Представлено наблюдение развития некрозов кожи пальцев рук у ребенка с врожденным пороком сердца спустя почти два года после начала терапии варфарином. Обсуждаются возможные причины осложнения и методы его лечения.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Финансирование: исследование не имело спонсорской поддержки.
Введение. Наиболее распространенными наследственными коагулопатиями являются гемофилия и болезнь Виллебранда. Часто под маской этих заболеваний скрываются редкие наследственные коагулопатии, в том числе наследственный дефицит фактора свертывания крови V (FV).
Цель: описание клинических проявлений и выбора тактики лечения у больных с наследственным дефицитом FV.
Основные сведения. Представлен обзор литературы и трех клинических наблюдений за больными с наследственным дефицитом FV. Обсуждаются вопросы дифференциальной диагностики наследственных коагулопатий, поскольку от точного диагноза зависит выбор гемостатической терапии. Больные с наследственным дефицитом FV требуют постоянного наблюдения гематологом с целью контроля спонтанного или индуцированного геморрагического синдрома, проведения гемостатической терапии при оперативных вмешательствах, беременности, родах.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Финансирование: исследование не имело спонсорской поддержки.
ОБМЕН ОПЫТОМ
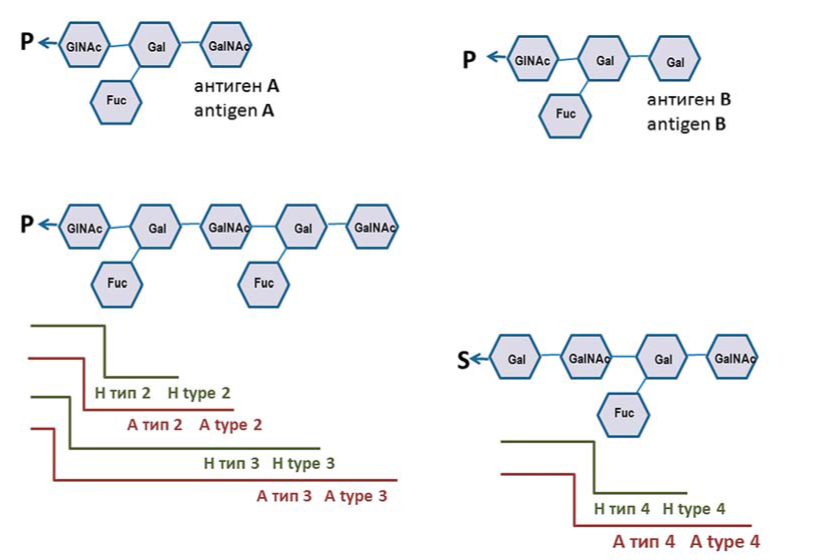
Введение. Определение слабых вариантов антигена А и их дифференциация необходимы для правильного подбора эритроцитсодержащих сред при гемотрансфузиях. Для этого в сочетании с реактивами анти-А, которые одинаково реагируют с антигенами А1 и А2, применяются селективные реактивы анти-А1, реагирующие только с антигеном А1 . Поскольку внутри самих подгрупп наблюдается вариабельность экспрессии антигена А, а установленного стандарта для реагентов и методик не существует, трактовка полученных результатов зачастую вызывает затруднения.
Цель: создать стратегию определения вариантов антигена А с применением доступных реагентов в реакции агглютинации.
Методы. Сравнение эффективности четырех анти-А1 - и двух анти-Н-реагентов проведено на 23 образцах крови с группой А2 и А2В и контрольных образцах А1 и А1 В. Использовались два типа анти-А1 -реагентов: лектин Dolychos biflorus и моноклональные антитела. Все реагенты предназначались для реакции прямой агглютинации. Принадлежность эритроцитов к подгруппе А2 была подтверждена генетическим анализом.
Результаты. Показано, что анти-А1 -реагенты не взаимодействовали с эритроцитами А2В, но часто реагировали с эритроцитами А2. Сила реакции с эритроцитами А2 сильно варьировала и была слабее, чем с А1 -эритроцитами, однако вызывала затруднения в установлении подгруппы. Одновременное тестирование с реагентом анти-Н позволяло сделать однозначный вывод о принадлежности крови к подгруппе: сильная реакция указывала на А2, отрицательная или слабая — на А1 . У двух доноров было отмечено расхождение результатов серологических и молекулярных методов исследования: серологически была определена подгруппа А3, генотипирование выявило аллель АВ0*А1 . В обоих случаях прямое секвенирование показало комбинацию мутантных аллелей, которая дает фенотип А3. При использовании коммерческих наборов для генотипирования методом полимеразной цепной реакции следует учитывать, что праймеры подобраны к наиболее часто встречающимся вариантам и не могут выявить все мутации гена АВ0.
Заключение. Надежная диагностика подгруппы А2 серологическими методами возможна с использованием лектина или моноклональных антител анти-А1 в сочетании с анти-H моноклональным реагентом.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Финансирование: исследование не имело спонсорской поддержки.
ISSN 2411-3042 (Online)